13.下列气体通入水中所得溶液呈碱性的是( )
| A. | CO2 | B. | SO2 | C. | NH3 | D. | HC1 |
12.下列化学用语表示正确的是( )
| A. | 乙酸的结构简式:C2H4O2 | |
| B. | 乙烯的电子式: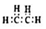 | |
| C. | 硫离子结构示意图: | |
| D. | 氢氧化钡的电离方程式:Ba(OH)2=Ba2++(OH-)2 |
11.2016年朝鲜又多次进行了核武和导弹试验,加剧了东亚及朝鲜半岛的紧张局势.${\;}_{92}^{235}$U是一种重要的核燃料,这里的“235”是指该原子的( )
| A. | 质子数 | B. | 中子数 | C. | 电子数 | D. | 质量数 |
10.下列过程中只涉及物理变化的是( )
| A. | 石油分馏 | B. | 煤的干馏 | C. | 海水制镁 | D. | 海带提碘 |
9.纯碱是一种非常重要的化工原料,纯碱属于( )
| A. | 碱 | B. | 盐 | C. | 氧化物 | D. | 有机物 |
7.二氧化硫的含量是空气质量监测的一个重要指标.
I.二氧化硫被雨水吸收后就形成了酸雨,某兴趣小组同学汲取热电厂附近的雨水进行实验.
①测得该雨水样品的pH为4.73;
②每隔1h,通过pH计测定雨水样品的pH,测得的结果如表:
根据以上信息,回答下列问题:
(1)正常雨水的pH为5.6,偏酸性,这是因为大气中的CO2溶于雨水.
(2)分析上述数据变化,你认为形成这一变化的原因是H2SO3与空气中的O2作用转化为H2SO4,使雨水的酸性增强,pH减小.
II.兴趣小组同学为测定空气中二氧化硫的体积分数,做了如下实验:取标准状况下的空气1.000L(内含氮气、氧气、二氧化硫、二氧化碳等),慢慢通过足量氯水,(反应的化学方程式为SO2+Br2+H2O=2HBr+H2SO4),在所得溶液中加入过量的氯化钡溶液,产生白色沉淀,将沉淀洗涤、干燥,称得其质量为0.233g.
(1)过滤时,除去沉淀中附着的过量氧化钡的方法是在漏斗中用蒸馏水淋洗.
(2)计算该空气样品中二氧化硫的体积分数(写出计算过程)
I.二氧化硫被雨水吸收后就形成了酸雨,某兴趣小组同学汲取热电厂附近的雨水进行实验.
①测得该雨水样品的pH为4.73;
②每隔1h,通过pH计测定雨水样品的pH,测得的结果如表:
| 测定时间/h | 0 | 1 | 2 | 3 | 4 |
| 雨水样品的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
(1)正常雨水的pH为5.6,偏酸性,这是因为大气中的CO2溶于雨水.
(2)分析上述数据变化,你认为形成这一变化的原因是H2SO3与空气中的O2作用转化为H2SO4,使雨水的酸性增强,pH减小.
II.兴趣小组同学为测定空气中二氧化硫的体积分数,做了如下实验:取标准状况下的空气1.000L(内含氮气、氧气、二氧化硫、二氧化碳等),慢慢通过足量氯水,(反应的化学方程式为SO2+Br2+H2O=2HBr+H2SO4),在所得溶液中加入过量的氯化钡溶液,产生白色沉淀,将沉淀洗涤、干燥,称得其质量为0.233g.
(1)过滤时,除去沉淀中附着的过量氧化钡的方法是在漏斗中用蒸馏水淋洗.
(2)计算该空气样品中二氧化硫的体积分数(写出计算过程)
5.下列离子方程式正确的是( )
| A. | 过氧化钠投入到水中:2Na2O2+2H2O=4Na++4OH-+O2↑ | |
| B. | 氯化铵溶液与浓NaOH 溶液加热:NH4++OH-=NH3•H2O | |
| C. | 氯化铝溶液中滴入过量氨水:Al3++3NH3•H2O=Al(OH)3↓+3 NH4+ | |
| D. | 实验室制取氯气:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$ Mn2++Cl2↑+2Cl-+2H2O |
4.设NA为阿伏加德罗常数的值,下列说法正确的是( )
0 161331 161339 161345 161349 161355 161357 161361 161367 161369 161375 161381 161385 161387 161391 161397 161399 161405 161409 161411 161415 161417 161421 161423 161425 161426 161427 161429 161430 161431 161433 161435 161439 161441 161445 161447 161451 161457 161459 161465 161469 161471 161475 161481 161487 161489 161495 161499 161501 161507 161511 161517 161525 203614
| A. | 2.3g钠与水反应产生组气的分子数为0.05NA | |
| B. | 28gN2和N4组成的混合气体中含有的原子数为3NA | |
| C. | 0.1 mol•L-1Na2SO4溶液含有0.1NA个SO42- | |
| D. | 22.4L氯气中含有的电子总数一定为34NA |