3.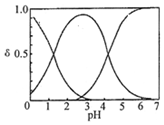 H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示[已知Ksp(CaC2O4)=2.3×10-9].下列说法正确的是( )
H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示[已知Ksp(CaC2O4)=2.3×10-9].下列说法正确的是( )
 H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示[已知Ksp(CaC2O4)=2.3×10-9].下列说法正确的是( )
H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示[已知Ksp(CaC2O4)=2.3×10-9].下列说法正确的是( )| A. | 0.1mol•L-1H2C2O4溶液使KMnO4溶液褪色的离子方程式:2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O | |
| B. | 0.1 mol•L-1 NaHC2O4溶液中:c(C2O42-)>c(H2C2O4) | |
| C. | pH=5时,溶液中主要含碳微粒浓度大小关系为:c(C2O42-)>c(H2C2O4)>c(HC2O4-) | |
| D. | 一定温度下,往CaC2O4饱和溶液中加入少量CaCl2固体,c(C2O42-)将减小,c(Ca2+)不变 |
2.下列说法中,不正确的是( )
| A. | 管道施工中,不能将铁制自来水管与铜制水龙头连接 | |
| B. | 化学反应过程中,一定有物质的变化,不一定有能量的变化 | |
| C. | 在配制的硫酸亚铁溶液中常加入一定量的铁粉和硫酸 | |
| D. | 已知C(石墨,s)═C(金刚石,s )△H>0,则石墨比金刚石稳定 |
1.对下列溶液的说法正确的是( )
| A. | pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1 | |
| B. | 浓度均为0.1 mol/L的四种溶液中由水电离出的H+浓度由大到小的顺序是:氯化铵、醋酸、硫酸、氢氧化钠 | |
| C. | 已知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12.某溶液中含有Cl-和CrO42-,浓度均为0.010mol•L-1,向该溶液中逐滴加入0.010 mol•L-1的AgNO3溶液时,CrO42-先沉淀 | |
| D. | 25℃时,取0.2mol•L-1 HClO溶液与0.2mol•L-1 NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,则c(Na+)-c(ClO-)=9.9×10-7mol•L-1 |
20.下列是哈伯法的流程图,其中为提高原料转化率而采取的措施是( )
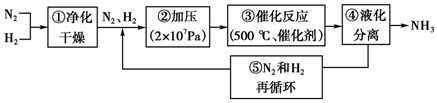

| A. | ①②③ | B. | ①③⑤ | C. | ②④ | D. | ②③④ |
19.下列关于环境问题的说法不正确的是( )
| A. | 用甘蔗生产的乙醇燃料属于可再生能源,利用乙醇燃料不会产生温室气体 | |
| B. | 低碳生活注重节能减排,尽量使用太阳能等代替化石燃料,可减少雾霾的发生 | |
| C. | 太阳能、风能和生物能源属于新能源 | |
| D. | 太阳能电池可将太阳能直接转化为电能 |
17.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 1 L 0.5 mol•L-1的Fe2(SO4)3 溶液中Fe3+的数目为NA | |
| B. | 室温下,pH=13的NaOH溶液中,OH-离子数目为0.1NA | |
| C. | 0.1 L 0.5 mol•L-1 CH3COOH溶液中含有的氢离子数目小于0.05NA | |
| D. | 电解精炼铜时,若阴极得到电子数为2NA个,则阳极质量减少64 g |
16.化学与社会、生活密切相关.下列现象或事实以及解释均正确的是( )
0 161320 161328 161334 161338 161344 161346 161350 161356 161358 161364 161370 161374 161376 161380 161386 161388 161394 161398 161400 161404 161406 161410 161412 161414 161415 161416 161418 161419 161420 161422 161424 161428 161430 161434 161436 161440 161446 161448 161454 161458 161460 161464 161470 161476 161478 161484 161488 161490 161496 161500 161506 161514 203614
| 选项 | 现象或事实 | 解释 |
| A | 在入海口的钢铁闸门上装一定数量的锌块可防止闸门被腐蚀 | 钢铁闸门与锌块在海水中构成原电池,钢铁闸门作正极 |
| B | 某些抗氧化剂作食品添加剂 | 抗氧化剂与食品反应,延缓食品腐败速率 |
| C | 用热的烧碱溶液洗去油污 | Na2CO3可直接与油污反应 |
| D | 明矾可作漂白剂 | 明矾电离出的Al3+水解时产生具有吸附性的胶体粒子 |
| A. | A | B. | B | C. | C | D. | D |
 某课外活动小组同学用图1装置进行实验,试回答下列问题:
某课外活动小组同学用图1装置进行实验,试回答下列问题: