题目内容
20.下列是哈伯法的流程图,其中为提高原料转化率而采取的措施是( )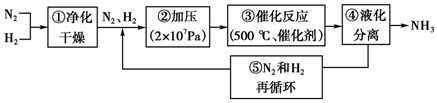
| A. | ①②③ | B. | ①③⑤ | C. | ②④ | D. | ②③④ |
分析 反应原理为N2(g)+3H2(g)$?_{催化剂}^{高温高压}$2NH3(g),△H<0,为提高原料转化率,应使平衡向正方向移动,可从压强、浓度、温度对平衡移动的影响的角度判断.
解答 解:反应原理为N2(g)+3H2(g)$?_{催化剂}^{高温高压}$2NH3(g),△H<0,为提高原料转化率,应使平衡向正方向移动,
根据方程式反应前后气体的化学计量数的关系可知增大压强有利于平衡向正方向移动;
正反应放热,升高温度不利用平衡向正反应方向移动,
催化剂对平衡移动无影响,
液化分离出氨气,可使生成物浓度减小,则可使平衡向正向移动,
氮气和氢气的再循环,可增大反应物浓度,有利于平衡向正向移动,
故选C.
点评 本题考查化学平衡的调控,为高频考点,侧重于外界条件对平衡移动的影响,题目难度中等,注意把握影响平衡移动的因素,分析反应的特点为解答该题的关键.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
10.下列关于物质分类的说法,正确的是( )
| A. | 碱性氧化物一定是金属氧化物,金属氧化物一定是碱性氧化物 | |
| B. | 由一种元素组成的物质一定是单质,两种元素组成的物质一定是化合物 | |
| C. | 非金属氧化物不一定是酸性氧化物,酸性氧化物不一定都是非金属氧化物 | |
| D. | 硫酸、纯碱、石膏是按酸、碱、盐排列的 |
11.下列说法正确的是( )
| A. | 试纸在使用时必须先要湿润 | |
| B. | 任何金属或者它们的化合物在火焰上灼烧都有特殊的焰色反应 | |
| C. | 在配制一定物质的量浓度溶液的定容步骤时,俯视凹液面,所配溶液浓度偏高 | |
| D. | 提纯混有少量硝酸钾的氯化钠,需经过溶解、蒸发浓缩、冷却结晶、过滤、洗涤、干燥等步骤 |
5.乙酸的下列性质中,可以证明它是弱电解质的是( )
| A. | 乙酸与水能以任意比例互溶 | |
| B. | 乙酸溶液的导电性弱 | |
| C. | 10 mL1 mol•L-1乙酸恰好与10 mL1 mol•L-1NaOH溶液完全反应 | |
| D. | 1 mol•L-1的乙酸溶液的C(H+)约为0.01 mol•L-1 |
8.对食物的酸、碱性判断正确的是( )
| A. | 柠檬是酸性食物 | B. | 猪肉、牛肉是碱性食物 | ||
| C. | 大多数的蔬菜和水果是碱性食物 | D. | 大米、面粉是碱性食物 |
9.用惰性电极电解下列溶液,电解一断时间后,阴极质量增加,电解液的pH下降的是( )
| A. | CuSO4 | B. | HCl | C. | BaCl2 | D. | Na2SO4 |
 ,反应中其还原剂是Na2O2.
,反应中其还原剂是Na2O2.