10. 已知 25℃时部分弱电解质的电离平衡常数数据如表:
已知 25℃时部分弱电解质的电离平衡常数数据如表:
回答下列问题:
(1)写出碳酸的主要的电离方程式H2CO3?H++HCO3-.若将碳酸饱和溶液稀释 10 倍,则稀释后的溶液中 c(H+)大于原来的十分之一(填“大于”、“小于”或“等于”).
(2)物质的量浓度均为 0.1mol/L 的五种溶液:pH 由小到大的顺序为e<a<d<c<b(用编号填写).
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3 e.NaSCN
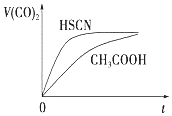
(3)25℃时,将 20mL0.1mol•L-1CH COOH 溶液和 20mL0.1mol•L-1HSCN 溶液分别与 20mL0.1mol•L-1NaHCO 溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图.反应初始阶段两种溶液产生 CO2气体的速率存在明显差异的原因是HSCN的酸性比CH3COOH强,其溶液中c(H+)较大,故其溶液与NaHCO3溶液的反应速率快反应结束后,假设 NaHCO3完全反应且气体全部逸出,则所得两溶液中,c(CH3COO)<c(SCN)(填“>”、“<”或“=”)
(4)25℃时,CH3COONa 与 CH3COOH 的混合溶液,若测得 pH=8,则溶液中c(Na+)-c(CH3COO-)=10-6-10-8mol/L(填代入数据后的计算式,不必算出具体数值).
(5)向 NaClO 溶液中通入少量的 CO2,发生反应的离子方程式为ClO-+CO2+H2O═HClO+HCO3-.
 已知 25℃时部分弱电解质的电离平衡常数数据如表:
已知 25℃时部分弱电解质的电离平衡常数数据如表:| 化学式 | HSCN | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.3×10-1 | 1.8×10-5 | Ka1=4.3×10-1Ka2=5.6×10-1 | 3.0×10-8 |
(1)写出碳酸的主要的电离方程式H2CO3?H++HCO3-.若将碳酸饱和溶液稀释 10 倍,则稀释后的溶液中 c(H+)大于原来的十分之一(填“大于”、“小于”或“等于”).
(2)物质的量浓度均为 0.1mol/L 的五种溶液:pH 由小到大的顺序为e<a<d<c<b(用编号填写).
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3 e.NaSCN
(3)25℃时,将 20mL0.1mol•L-1CH COOH 溶液和 20mL0.1mol•L-1HSCN 溶液分别与 20mL0.1mol•L-1NaHCO 溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图.反应初始阶段两种溶液产生 CO2气体的速率存在明显差异的原因是HSCN的酸性比CH3COOH强,其溶液中c(H+)较大,故其溶液与NaHCO3溶液的反应速率快反应结束后,假设 NaHCO3完全反应且气体全部逸出,则所得两溶液中,c(CH3COO)<c(SCN)(填“>”、“<”或“=”)
(4)25℃时,CH3COONa 与 CH3COOH 的混合溶液,若测得 pH=8,则溶液中c(Na+)-c(CH3COO-)=10-6-10-8mol/L(填代入数据后的计算式,不必算出具体数值).
(5)向 NaClO 溶液中通入少量的 CO2,发生反应的离子方程式为ClO-+CO2+H2O═HClO+HCO3-.
9.根据下列实验事实,不能得到相应结论的是( )
| 选项 | 实验操作和现象 | 结论 |
| A | 向2mol/L的醋酸溶液中加入镁条,产生气泡的速率先加快再减慢 | 反应刚开始时,醋酸电离平衡正移,c(H+)增大 |
| B | 常温下分别测等浓度的醋酸和氨水pH,发现二者的pH之和为14 | 常温下,醋酸和氨水的电离平衡常数相等 |
| C | 向均盛有2mL5%H2O溶液的两支试管中分别滴入0.2mol/LFe3+,和0.3mol/LCu2+溶液1mL,前者生成气泡的速率更快 | 催化效果:Fe3+>Cu2+ |
| D | 向硼酸(H3BO3)溶液中滴加少量Na2CO3溶液,观察到无明显现象 | H3BO3的酸性弱于H2CO3 |
| A. | A | B. | B | C. | C | D. | D |
8.下列有关问题,与盐的水解无关的是( )
| A. | NH4Cl 与 ZnCl2溶液可作焊接金属中的除锈剂 | |
| B. | 用 NaHSO4去除暖手瓶中的水垢 | |
| C. | 实验室盛放 Na2CO3溶液的试剂瓶不能用磨口玻璃塞 | |
| D. | 加热蒸干 AlCl3溶液得到 Al(OH)3固体 |
7.下列条件下,对应离子一定能大量共存的是( )
| A. | 在0.1mol/LNaHCO3溶液中:Al3+、NH4+、SO42-、NO3- | |
| B. | 常温下,$\frac{{K}_{W}}{c({H}^{+})}$=0.1mol/L的溶液中:K+,Cl-,Fe2+,NO3- | |
| C. | 使甲基橙变红的溶液中:NH4+,Cl-,SO2-,Mg2+ | |
| D. | 25℃时,水电离出的c(H+)=1×10-13mol/L:K+,Ba2+,NO3-,S2- |
6.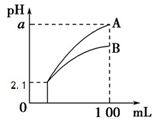 pH=2.1 的两种酸溶液 A、B 各 1mL,分别加水稀释到 100mL,其 pH 与溶液体积的关系如图,下列说法不正确的是( )
pH=2.1 的两种酸溶液 A、B 各 1mL,分别加水稀释到 100mL,其 pH 与溶液体积的关系如图,下列说法不正确的是( )
 pH=2.1 的两种酸溶液 A、B 各 1mL,分别加水稀释到 100mL,其 pH 与溶液体积的关系如图,下列说法不正确的是( )
pH=2.1 的两种酸溶液 A、B 各 1mL,分别加水稀释到 100mL,其 pH 与溶液体积的关系如图,下列说法不正确的是( )| A. | 若 a<4.1,则 A、B都是弱酸 | |
| B. | 稀释后,A 酸溶液的酸性比B酸溶液强 | |
| C. | 若 a=4.1,则 A 是强酸,B是弱酸 | |
| D. | A、B两种酸溶液的物质的量浓度一定相等 |
5.一定条件下存在反应:H2(g)+I2(g)?2HI(g)△H<0,现有三个相同的体积均为 1L 的恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入 1mol H2和 1molI2(g),在Ⅱ中充入 2molHI(g),在Ⅲ中充入 2mol H2和2mol I2(g),700℃条件下开 始反应.达到平衡时,下列说法正确的是( )
| A. | 容器Ⅰ、Ⅱ中正反应速率相同 | |
| B. | 容器Ⅰ中反应的平衡常数大于容器Ⅲ中反应的平衡常数 | |
| C. | 容器Ⅱ中的气体颜色比容器Ⅰ中的气体颜色深 | |
| D. | 容器Ⅰ中 H2的转化率与容器Ⅱ中HI的转化率之和等于1 |
4. 如图表示两个常见固氮反应的平衡常数对数值(lgK)与温度的关系:
如图表示两个常见固氮反应的平衡常数对数值(lgK)与温度的关系:
①N2+3H2?2NH3;②N2+O2?2NO
根据图中的数据判断下列说法正确的是( )
 如图表示两个常见固氮反应的平衡常数对数值(lgK)与温度的关系:
如图表示两个常见固氮反应的平衡常数对数值(lgK)与温度的关系:①N2+3H2?2NH3;②N2+O2?2NO
根据图中的数据判断下列说法正确的是( )
| A. | 只有反应①是放热反应 | |
| B. | 升温,反应①的速率减小反应②的速率增大 | |
| C. | 可以在常温下利用反应①进行工业固氮 | |
| D. | 曲线的交点表示反应①和反应②体系中 N2 的转化率相等 |
3.已知 X2(g)+Y2 (g)?2Z(g),X2、Y2、Z 的起始浓度分别为 0,1mol•L-1、0.3mol•L-1,0.2mol•L-1.在一定条件下,当反应达到平衡时,各物质的浓度可能是( )
| A. | Z 为 0.4mol•L-1 | B. | X 为 0.2 mol•L-1 | ||
| C. | Y 为 0.4 mol•L-1 | D. | Z 为 0.3 mol•L-1 |
2.对 N2+3H2?2NH3 反应,仅改变下列一个条件,就能提高活化分子的浓度从而加快正反应速率的是 ( )
| A. | 加热 | B. | 增大体积 | C. | 加负催化剂 | D. | 补充 He |
1.配制一定体积、一定物质的量浓度的溶液,实验结果产生偏高影响的是( )
0 161254 161262 161268 161272 161278 161280 161284 161290 161292 161298 161304 161308 161310 161314 161320 161322 161328 161332 161334 161338 161340 161344 161346 161348 161349 161350 161352 161353 161354 161356 161358 161362 161364 161368 161370 161374 161380 161382 161388 161392 161394 161398 161404 161410 161412 161418 161422 161424 161430 161434 161440 161448 203614
| A. | 容量瓶中原有少量蒸馏水 | B. | 溶解所用的烧杯未洗涤 | ||
| C. | 定容时仰视观察液面 | D. | 定容时俯视观察液面 |