题目内容
6.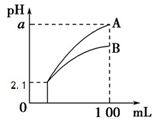 pH=2.1 的两种酸溶液 A、B 各 1mL,分别加水稀释到 100mL,其 pH 与溶液体积的关系如图,下列说法不正确的是( )
pH=2.1 的两种酸溶液 A、B 各 1mL,分别加水稀释到 100mL,其 pH 与溶液体积的关系如图,下列说法不正确的是( )| A. | 若 a<4.1,则 A、B都是弱酸 | |
| B. | 稀释后,A 酸溶液的酸性比B酸溶液强 | |
| C. | 若 a=4.1,则 A 是强酸,B是弱酸 | |
| D. | A、B两种酸溶液的物质的量浓度一定相等 |
分析 由图可知,稀释相同的倍数,A的变化大,则A的酸性比B的酸性强,溶液中氢离子浓度越大,酸性越强,对于一元强酸来说c(酸)=c(H+),但对于一元弱酸,c(酸)>c(H+),以此来解答.
解答 解:A.pH=2.1的酸,加水稀释到100倍,若pH=4.1,为强酸,若 a<4.1,则 A、B都是弱酸,故A正确;
B.由图可知,B的pH小,c(H+)大,则B酸的酸性强,故B错误;
C.pH=2.1的酸,加水稀释到100倍,若pH=4.1,A是强酸,B的pH变化小,则B为弱酸,故C正确;
D.因A、B酸的强弱不同,一元强酸来说c(酸)=c(H+),对于一元弱酸,c(酸)>c(H+),则A、B两种酸溶液的物质的量浓度不一定相等,故D错误;
故选BD.
点评 本题考查酸的稀释及图象,明确强酸在稀释时pH变化程度大及酸的浓度与氢离子的浓度的关系是解答本题的关键,难度不大.

练习册系列答案
相关题目
17.对于X+Y(s)?Z的平衡体系,若增大压强,Y的平衡转化率增大,则X和Z可能的状态是( )
| A. | X为气态,Z为固态 | B. | X为固态,Z为气态 | C. | X为气态,Z为气态 | D. | X为固态,Z为固态 |
14.合成药物异搏定路线中某一步骤如图所示,下列说法正确的是( )


| A. | 物质X的分子式为C8H10O2 | |
| B. | 物质Y可以发生水解、加成和氧化反应 | |
| C. | 物质Z中所有原子有可能在同一平面内 | |
| D. | 物质X的同分异构体中含苯环且能水解的共有6种 |
1.配制一定体积、一定物质的量浓度的溶液,实验结果产生偏高影响的是( )
| A. | 容量瓶中原有少量蒸馏水 | B. | 溶解所用的烧杯未洗涤 | ||
| C. | 定容时仰视观察液面 | D. | 定容时俯视观察液面 |
18.现有三组溶液,①汽油和氯化钠溶液,②39%的乙醇溶液,③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
| A. | 分液 萃取 蒸馏 | B. | 萃取 蒸馏 分液 | ||
| C. | 分液 蒸馏 萃取 | D. | 蒸馏 萃取 分液 |
16.下列关于淀粉和纤维素的叙述中,正确的是( )
| A. | 它们都是混合物 | B. | 它们都是天然高分子化合物 | ||
| C. | 它们互为同分异构体 | D. | 它们水解的最终产物都是葡萄糖 |