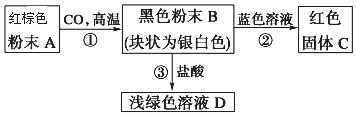
6.通过α粒子轰击金箔的实验现象,否定葡萄干面包原子模型的科学家是( )
| A. | 伦琴 | B. | 卢瑟福 | C. | 道尔顿 | D. | 汤姆孙 |
5.相同温度下,2H2(g)+O2(g)=2H2O(g)+akJ;2H2(g)+O2(g)=2H2O(l)+bkJ,两个反应放出的热量a与b的关系是( )
| A. | a<b | B. | a>b | C. | a=b | D. | 2b=a |
4.25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A. | pH=2的HA溶液与pH=12的MOH碱溶液以任意比混合:c(H+)+c(M+)═c(OH-)+c(A-) | |
| B. | 0.1mol•L-1Na2SO3溶液:c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3) | |
| C. | 等浓度、等体积的Na2CO3和NaHCO3混合溶液:$\frac{c{(HCO}_{3}^{-})}{c({H}_{2}C{O}_{3})}>$$\frac{c{(CO}_{3}^{2-})}{c{(HCO}_{3}^{-})}$ | |
| D. | 0.1mol•L-1CH3COONa溶液与0.1mol•L-1CaCl2溶液等体积混合:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(CL-) |
3.一定温度下,在三个体积均为1.0L的恒容密闭容器中充入一定量的H2和SO2,发生下列反应:3H2(g)+SO2(g)?2H2O(g)+H2S(g).下列说法正确的是( )
| 容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||
| H2 | SO2 | H2 | SO2 | ||
| 容器Ⅰ | 300 | 0.3 | 0.1 | / | 0.02 |
| 容器Ⅱ | 300 | 0.6 | 0.2 | / | / |
| 容器Ⅲ | 240 | 0.3 | 0.1 | / | 0.01 |
| A. | 该反应的正反应吸热 | |
| B. | 到达平衡时,容器Ⅰ中SO2的转化率比容器Ⅱ的大 | |
| C. | 240℃时,该反应的平衡常数为1.08×104 | |
| D. | 到达平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的大 |
2.Fe(OH)3可用来制颜料、药物,作净水剂.现设计实验研究制备Fe(OH)3的方法.
资料:新制Fe(OH)3在溶液中存在两种电离:Fe3++3OH-?Fe(OH)3?H++FeO2-+H2O
(1)向3支盛有1mL 1.0mol•L-1 FeCl3溶液的试管中,分别加入3mL不同浓度的NaOH溶液,都产生红褐色沉淀.充分反应后,过滤,取滤液分成两等份,分别进行实验,实验记录如表:
①产生红褐色沉淀的离子方程式是Fe3++3OH-?Fe(OH)3↓.
②当c(NaOH)≥6.0 mol•L-1时,实验Ⅱ中溶液变红的原因是FeO2-+4H+?Fe3++2H2O、Fe3++3SCN-?Fe(SCN)3(用离子方程式表示).
(2)有同学提出可用某些盐与FeCl3反应制备Fe(OH)3.
①向1mL 1.0mol•L-1 FeCl3溶液中滴加1.0mol•L-1Na2CO3溶液,立即有大量气泡并有红褐色沉淀产生.有同学提出沉淀中可能含有碳酸盐.将沉淀过滤、洗涤后取样,加入少量稀盐酸,有无色气体产生,证明沉淀中含有碳酸盐.
②向1mL 1.0mol•L-1FeCl3溶液中滴加1.0mol•L-1Na2SO3溶液,溶液由黄色变为红色,无丁达尔效应,继续滴加Na2SO3溶液,最终得到红褐色沉淀.经检验沉淀中除Fe(OH)3外还含有FeSO3.产生FeSO3的原因是2Fe3++SO32-+H2O?2Fe2++SO42-+2H+、Fe2++SO32-?FeSO3↓.
(3)比较(1)和(2),制备Fe(OH)3的合理方法是1mL1.0mol•L-1FeCl3溶液与3mL浓度小于6.0mol•L-1的NaOH溶液(注明试剂和用量).
(4)FeSO4溶液仅与一种试剂反应也可制Fe(OH)3,该试剂的化学式是NaClO(写出一种即可).
资料:新制Fe(OH)3在溶液中存在两种电离:Fe3++3OH-?Fe(OH)3?H++FeO2-+H2O
(1)向3支盛有1mL 1.0mol•L-1 FeCl3溶液的试管中,分别加入3mL不同浓度的NaOH溶液,都产生红褐色沉淀.充分反应后,过滤,取滤液分成两等份,分别进行实验,实验记录如表:
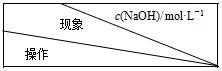 | 5.0 | 6.0 | 7.0 |
| 实验Ⅰ:滴入几滴KSCN溶液 | 不变红 | 不变红 | 不变红 |
| 实验Ⅱ:先加入过量稀硫酸,再滴入几滴KSCN溶液 | 不变红 | 变红 | 变红 |
②当c(NaOH)≥6.0 mol•L-1时,实验Ⅱ中溶液变红的原因是FeO2-+4H+?Fe3++2H2O、Fe3++3SCN-?Fe(SCN)3(用离子方程式表示).
(2)有同学提出可用某些盐与FeCl3反应制备Fe(OH)3.
①向1mL 1.0mol•L-1 FeCl3溶液中滴加1.0mol•L-1Na2CO3溶液,立即有大量气泡并有红褐色沉淀产生.有同学提出沉淀中可能含有碳酸盐.将沉淀过滤、洗涤后取样,加入少量稀盐酸,有无色气体产生,证明沉淀中含有碳酸盐.
②向1mL 1.0mol•L-1FeCl3溶液中滴加1.0mol•L-1Na2SO3溶液,溶液由黄色变为红色,无丁达尔效应,继续滴加Na2SO3溶液,最终得到红褐色沉淀.经检验沉淀中除Fe(OH)3外还含有FeSO3.产生FeSO3的原因是2Fe3++SO32-+H2O?2Fe2++SO42-+2H+、Fe2++SO32-?FeSO3↓.
(3)比较(1)和(2),制备Fe(OH)3的合理方法是1mL1.0mol•L-1FeCl3溶液与3mL浓度小于6.0mol•L-1的NaOH溶液(注明试剂和用量).
(4)FeSO4溶液仅与一种试剂反应也可制Fe(OH)3,该试剂的化学式是NaClO(写出一种即可).
18.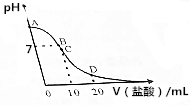 25℃,在20mL0.1mol•L-1氨水溶液中逐滴加入0.2mol•L-1HCl溶液,溶液的pH与所加盐酸的体积关系如图所示,已知0.1mol•L-1氨水的电离度为1.32%.下列说法不正确的是( )
25℃,在20mL0.1mol•L-1氨水溶液中逐滴加入0.2mol•L-1HCl溶液,溶液的pH与所加盐酸的体积关系如图所示,已知0.1mol•L-1氨水的电离度为1.32%.下列说法不正确的是( )
0 161231 161239 161245 161249 161255 161257 161261 161267 161269 161275 161281 161285 161287 161291 161297 161299 161305 161309 161311 161315 161317 161321 161323 161325 161326 161327 161329 161330 161331 161333 161335 161339 161341 161345 161347 161351 161357 161359 161365 161369 161371 161375 161381 161387 161389 161395 161399 161401 161407 161411 161417 161425 203614
 25℃,在20mL0.1mol•L-1氨水溶液中逐滴加入0.2mol•L-1HCl溶液,溶液的pH与所加盐酸的体积关系如图所示,已知0.1mol•L-1氨水的电离度为1.32%.下列说法不正确的是( )
25℃,在20mL0.1mol•L-1氨水溶液中逐滴加入0.2mol•L-1HCl溶液,溶液的pH与所加盐酸的体积关系如图所示,已知0.1mol•L-1氨水的电离度为1.32%.下列说法不正确的是( )| A. | 在A点处的溶液中pH<12 | B. | 在B点:c(NH4+)=c(Cl-)>c(OH-)>c(H+) | ||
| C. | 在C点:c(Cl-)>c(NH4+)>c(H+)>c(OH-) | D. | 在D点:c(NH4+)+c(NH3•H2O)=2c(Cl-) |

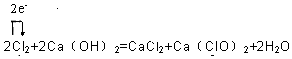 ,并用单线桥表示该反应电子转移的方向和数目.
,并用单线桥表示该反应电子转移的方向和数目. (任填一种物质的电子式)
(任填一种物质的电子式)