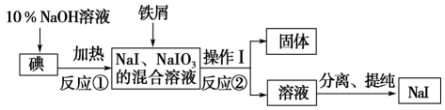
3.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 含有NA个原子的氢气在标准状况下的体积约为22.4 L | |
| B. | 25℃,1.01×105 Pa,64 g SO2中含有的原子数为3NA | |
| C. | 常温常压下,32gO2和32g O3所含氧原子数分别是2NA和3NA | |
| D. | Na2O2与CO2反应每生成1mol O2时所转移的电子数为4NA |
2.如图所示,下列实验操作方法正确的是( )
| A. |  检测容量瓶是否漏水的方法 | B. |  给溶液加热 | ||
| C. |  放回滴瓶 | D. | 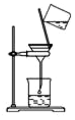 过滤 |
18.某溶液中含有 HCO3-、CO32-、Na+、NO3-四种离子,若向其中加入 Na2O2 粉末,充分反应后(溶液体积变化忽略不计),溶液中离子浓度保持不变的是( )
| A. | CO32- | B. | CO32-、NO3- | C. | NO3- | D. | CO32-、NO3-、Na+ |
17.下列离子能大量共存,而且加入 Al 后能产生氢气的是( )
| A. | H+、Mg2+、Al3+、CO32- | B. | Na+、K+、Cl-、Ba2+ | ||
| C. | H+、Fe3+、Cl-、SCN- | D. | OH-、Ba2+、Cl-、NO${\;}_{3}^{-}$ |
16.下列离子方程式书写正确的是( )
| A. | 钠和冷水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 铝粉投入到 NaOH 溶液中:2Al+2OH-═2AlO2-+H2↑ | |
| C. | 铁粉与稀硫酸溶液反应:2Fe+6H+═2Fe3++3H2↑ | |
| D. | Cl2 与烧碱溶液跟反应:Cl2+2OH-═Cl-+ClO-+H2O |
15.某下组同学欲研究SO2的性质.
(1)将相关的含硫物质分为如下表所示3组.第3组中物质X的化学式是H2SO4.
(2)利用如图所示的装置研究SO2的性质:
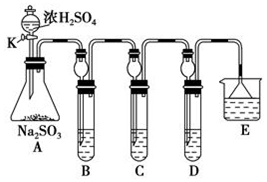
①在B中检验SO2的氧化性,则B中发生的化学反应方程式:SO2+2H2S=3S↓+2H2O.
②在C中装KMnO4溶液,目的是检验SO2的还原性,溶液逐渐褪色.生成Mn2+.同时pH降低.则C中反应的离子方程式为5SO2+2H2O+2MnO4-=5SO42-+2Mn2++4H+.
③在D中有40mL2.5mol/LNaOH溶液,反应后增重4,则装置D中发生反应的总化学方程式是5SO2+8NaOH=3Na2SO3+2NaHSO3+3H2O.
0 161163 161171 161177 161181 161187 161189 161193 161199 161201 161207 161213 161217 161219 161223 161229 161231 161237 161241 161243 161247 161249 161253 161255 161257 161258 161259 161261 161262 161263 161265 161267 161271 161273 161277 161279 161283 161289 161291 161297 161301 161303 161307 161313 161319 161321 161327 161331 161333 161339 161343 161349 161357 203614
(1)将相关的含硫物质分为如下表所示3组.第3组中物质X的化学式是H2SO4.
| 第1组 | 第2组 | 第3组 |
| S(单质) | SO2、H2SO4、Na2SO3、NaHSO3 | SO3、X、Na2SO4、NaHSO4 |

①在B中检验SO2的氧化性,则B中发生的化学反应方程式:SO2+2H2S=3S↓+2H2O.
②在C中装KMnO4溶液,目的是检验SO2的还原性,溶液逐渐褪色.生成Mn2+.同时pH降低.则C中反应的离子方程式为5SO2+2H2O+2MnO4-=5SO42-+2Mn2++4H+.
③在D中有40mL2.5mol/LNaOH溶液,反应后增重4,则装置D中发生反应的总化学方程式是5SO2+8NaOH=3Na2SO3+2NaHSO3+3H2O.