10.下列不能用勒夏特列原理解释的是( )
①盛满二氧化氮的烧瓶浸入热水中颜色变深
②新制的氯水在光照条件下颜色变浅
③在H2、I2(g)和HI组成的平衡体系中,加压,混合气体颜色变深
④饱和FeCl3溶液滴入沸水中可制得氢氧化铁胶体
⑤高锰酸钾(KMnO4)溶液加水稀释后颜色变浅
⑥加催化剂有利于氨氧化反应
⑦500℃左右比室温更有利于合成氨的反应
⑧收集氯气用排饱和食盐水的方法
⑨可用浓氨水和氢氧化钠固体快速制取氨气.
①盛满二氧化氮的烧瓶浸入热水中颜色变深
②新制的氯水在光照条件下颜色变浅
③在H2、I2(g)和HI组成的平衡体系中,加压,混合气体颜色变深
④饱和FeCl3溶液滴入沸水中可制得氢氧化铁胶体
⑤高锰酸钾(KMnO4)溶液加水稀释后颜色变浅
⑥加催化剂有利于氨氧化反应
⑦500℃左右比室温更有利于合成氨的反应
⑧收集氯气用排饱和食盐水的方法
⑨可用浓氨水和氢氧化钠固体快速制取氨气.
| A. | ②③⑤⑥ | B. | ③⑤⑥⑨ | C. | ③⑤⑥⑦ | D. | ④⑥⑦⑨ |
9.下列说法正确的是( )
| A. | 地下钢管连接锌板属于牺牲阳极的阴极保护法 | |
| B. | 放热反应的反应速率总是大于吸热反应的反应速率 | |
| C. | 化学平衡发生移动,平衡常数一定发生改变 | |
| D. | 强电解质溶液导电能力一定很强,弱电解质溶液导电能力一定很弱 |
8.某化学反应的△H=-122kJ•mol-1,△S=+231J•mol-1•K-1,则此反应在下列哪种情况下可自发进行( )
| A. | 在任何温度下都能自发进行 | B. | 在任何温度下都不能自发进行 | ||
| C. | 仅在高温下自发进行 | D. | 仅在低温下自发进行 |
7.下列装置所示的实验中,能达到实验目的是( )
| A. | 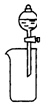 从Mg(OH)2悬浊液中分离出Mg(OH)2 | B. | 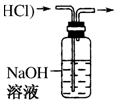 除去HCl中的SO2 | ||
| C. | 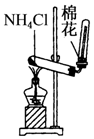 实验室制氨气 | D. | 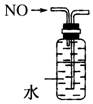 排水法收集NO |
6.下列反应中生成H2的速率最快的是( )
| 金属 | 酸溶液 | 温度 | |
| A | Mg | 0.5mol•L-1 H2SO4 | 20℃ |
| B | Mg | 1mol•L-1 H2SO4 | 30℃ |
| C | Zn | 2mol•L-1 HCl | 20℃ |
| D | Fe | 1mol•L-1 HCl | 20℃ |
| A. | A | B. | B | C. | C | D. | D |
5.下列陈述ⅠⅡ正确并且有因果关系的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2有漂白性 | SO2可使溴水褪色 |
| B | SiO2有导电性 | SiO2可用于制备光导纤维 |
| C | 浓硫酸有吸水性 | 浓硫酸可用于干燥H2和NH3 |
| D | Fe3+有强氧化性 | FeCl3溶液可用于回收废旧电路板中的铜 |
| A. | A | B. | B | C. | C | D. | D |
4.下列实验能证明一定有二氧化硫存在的是( )
①能使澄清石灰水变浑浊;
②能使湿润的蓝色石蕊试纸变红;
③能使品红溶液褪色;
④通入足量的氢氧化钠溶液再加BaCl2溶液有白色沉淀产生,该沉淀溶于稀盐酸;
⑤通入气体能使溴水褪色,再滴加Ba(NO3)2溶液有白色沉淀产生.
①能使澄清石灰水变浑浊;
②能使湿润的蓝色石蕊试纸变红;
③能使品红溶液褪色;
④通入足量的氢氧化钠溶液再加BaCl2溶液有白色沉淀产生,该沉淀溶于稀盐酸;
⑤通入气体能使溴水褪色,再滴加Ba(NO3)2溶液有白色沉淀产生.
| A. | 只有⑤ | B. | 均能 | C. | ③④⑤ | D. | 均不能 |
3.下列观点正确的是( )
| A. | 某单质固体能导电,该单质一定是金属 | |
| B. | 某元素原子最外层只有一个电子,该元素一定属于金属元素 | |
| C. | 某纯净物在常温常压下为气体,则组成该物质的微粒一定含共价键 | |
| D. | 某化合物熔融态能导电,该化合物中一定有离子键 |
2.设NA为阿伏加德罗常数的值.下列说法正确的是( )
0 161112 161120 161126 161130 161136 161138 161142 161148 161150 161156 161162 161166 161168 161172 161178 161180 161186 161190 161192 161196 161198 161202 161204 161206 161207 161208 161210 161211 161212 161214 161216 161220 161222 161226 161228 161232 161238 161240 161246 161250 161252 161256 161262 161268 161270 161276 161280 161282 161288 161292 161298 161306 203614
| A. | 1mol的氢氧根离子中的电子数目约为9NA | |
| B. | 56 g铁片投入足量稀H2SO4中生成NA个SO2分子 | |
| C. | 标准状况下,11.2 L NH3中含有分子的数目为0.5NA | |
| D. | 在铜与足量稀硝酸的反应中,每生成0.1 mol气体,转移电子的数目为0.2NA |