题目内容
3.下列观点正确的是( )| A. | 某单质固体能导电,该单质一定是金属 | |
| B. | 某元素原子最外层只有一个电子,该元素一定属于金属元素 | |
| C. | 某纯净物在常温常压下为气体,则组成该物质的微粒一定含共价键 | |
| D. | 某化合物熔融态能导电,该化合物中一定有离子键 |
分析 A.能导电的单质不一定为金属单质,有些非金属单质也导电;
B.H原子的最外层只有一个电子;
C.稀有气体为单原子分子;
D.离子化合物在熔融状态能电离,共价化合物在熔融时不能电离.
解答 解:A.能导电的单质不一定为金属单质,有些非金属单质也导电,如石墨能导电,故A错误;
B.H原子的最外层只有一个电子,所以某元素原子最外层只有一个电子,该元素不一定属于金属元素,故B错误;
C.稀有气体为单原子分子,分子中不存在共价键,故C错误;
D.离子化合物在熔融状态能电离,共价化合物在熔融时不能电离,所以某化合物熔融态能导电,该化合物中一定有离子键,故D正确.
故选D.
点评 本题考查了物质的导电性、电子排布、化学键、离子化合物和共价化合物,题目涉及的知识点较多,侧重于基础知识的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.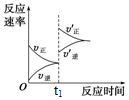 如图为化学反应3A(g)?B(g)+C(g),△H<0在一密闭容器中反应的速率-时间图,下列叙述符合此图所给信息的是( )
如图为化学反应3A(g)?B(g)+C(g),△H<0在一密闭容器中反应的速率-时间图,下列叙述符合此图所给信息的是( )
 如图为化学反应3A(g)?B(g)+C(g),△H<0在一密闭容器中反应的速率-时间图,下列叙述符合此图所给信息的是( )
如图为化学反应3A(g)?B(g)+C(g),△H<0在一密闭容器中反应的速率-时间图,下列叙述符合此图所给信息的是( )| A. | t1 时,向容器中通入一定量的A气体 | |
| B. | t1 时,缩小容器的体积 | |
| C. | t1 时,升高体系温度 | |
| D. | 从t1 开始到新的平衡的过程中,平衡向逆反应方向移动 |
11.已知室温下,0.1mol/L的NaHSO3溶液的pH=4.该溶液中各粒子的浓度关系正确的是( )
| A. | c(Na+)>c(HSO3-)>c(H+)>c(OH-) | B. | c(H2SO3)>c(SO32-) | ||
| C. | c(H+)+c(Na+)=c(OH-)+c(SO32-)+c(HSO3-) | D. | c(Na+)=c(HSO3-)+c(H2SO3)+2 c(SO32-) |
18.化学与环境密切相关,下列有关说法不正确的是 ( )
| A. | CO2不属于大气污染物 | |
| B. | 酸雨是pH小于7的雨水 | |
| C. | CO2、NO2或SO2都会导致酸雨的形成 | |
| D. | 大气中CO2含量的增加会导致温室效应加剧 |
8.某化学反应的△H=-122kJ•mol-1,△S=+231J•mol-1•K-1,则此反应在下列哪种情况下可自发进行( )
| A. | 在任何温度下都能自发进行 | B. | 在任何温度下都不能自发进行 | ||
| C. | 仅在高温下自发进行 | D. | 仅在低温下自发进行 |
12.一包白色粉末,可能含有Na2CO3、CaCl2、NaI、CuSO4中的一种或几种,把它溶于水得无色澄清溶液,再加入用硝酸酸化的AgNO3溶液,有气体和沉淀产生,则原来的白色粉末( )
| A. | CaCl2,、Na2CO3 | B. | Na2CO3、NaI | ||
| C. | CaCl2、Na2CO3、NaI | D. | CaCl2、NaI |