题目内容
2.设NA为阿伏加德罗常数的值.下列说法正确的是( )| A. | 1mol的氢氧根离子中的电子数目约为9NA | |
| B. | 56 g铁片投入足量稀H2SO4中生成NA个SO2分子 | |
| C. | 标准状况下,11.2 L NH3中含有分子的数目为0.5NA | |
| D. | 在铜与足量稀硝酸的反应中,每生成0.1 mol气体,转移电子的数目为0.2NA |
分析 A.氢氧根离子中含有10个电子,1mol氢氧根离子含有10mol电子;
B.铁与稀硫酸反应生成的是氢气;
C.根据n=$\frac{V}{{V}_{m}}$计算出氨气的物质的量,然后根据N=nNA计算出含有分子数;
D.铜与稀硝酸反应生成的是NO,生成0.1molNO转移0.3mol电子.
解答 解:A.1mol的氢氧根离子中含有10mol电子,含有的电子数目约为10NA,故A错误;
B.56 g铁片投入足量稀H2SO4中,反应生成的是氢气,不会生成二氧化硫气体,故B错误;
C.标准状况下,11.2 L NH3的物质的量为:$\frac{11.2L}{22.4L/mol}$=0.5mol,含有正确分子的数目为0.5NA,故C正确;
D.在铜与足量稀硝酸的反应生成NO气体,每生成0.1 mol NO气体转移电子的物质的量为:0.1mol×(5-2)=0.3mol,转移电子的数目为0.3NA,故D错误;
故选C.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,试题有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
13.下列反应中,改变反应物的用量、条件或浓度,不会改变生成物的是( )
| A. | 铜和硝酸反应 | B. | 二氧化碳通入氢氧化钠溶液中 | ||
| C. | 细铁丝在氯气中燃烧 | D. | 铁和与硫酸溶液反应 |
10.已知Ksp(AgCl)=1.56×10-10,Ksp(AgBr)=7.7×10-13,Ksp(Ag2CrO4)=9.0×10-12.某溶液中含有Cl-,Br-,CrO4-,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为( )
| A. | I-、Br-、CrO4- | B. | Br-、Cl-、CrO4- | C. | CrO4-、Br-、I- | D. | Br-、CrO4-、Cl- |
17.在硫酸铁溶液中,加入ag铜完全溶解后再加入bg铁,充分反应后得到cg残余固体,且a>c,则下列说法中正确的是( )
| A. | 残余固体可能为铁和铜的混合物 | |
| B. | 最后得到的溶液可能含有Fe3+ | |
| C. | 残余固体是铁,溶液中一定不含Cu2+ | |
| D. | 残余固体一定全部是铜 |
7.下列装置所示的实验中,能达到实验目的是( )
| A. | 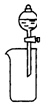 从Mg(OH)2悬浊液中分离出Mg(OH)2 | B. | 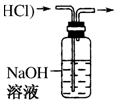 除去HCl中的SO2 | ||
| C. | 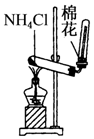 实验室制氨气 | D. | 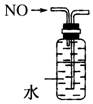 排水法收集NO |
11.设NA为阿伏伽德罗常数的值,下列有关说法不正确的是( )
| A. | 常温常压下,8gCH4中含有的氢原子数为2NA | |
| B. | 含有NA个氦原子的氦气在标准状况下的体积约为22.4L | |
| C. | 常温常压下,48氧气和臭氧(O3)混合物中所含氧原子总数为3NA | |
| D. | 物质的量浓度为0.5 mol•L-1的MgCl2溶液中,含有Cl-个数为1NA |