12.下列物质依次按照混合物、氧化物、弱电解质和非电解质的顺序排列的一组是( )
| A. | 淀粉、CuO、HClO、Cu | |
| B. | 水玻璃、Na2O、CaO•6SiO2、AgO、SO3 | |
| C. | KAl (SO4) 2•12H2O、KCIO3、NH3•H2O、CH3CH2OH | |
| D. | 普通玻璃、H2O、Fe (SCN) 3、葡萄糖 |
11.下列说法不正确的是( )
| A. | 浙大研制的石墨烯弹性气凝胶(又名碳海绵)入选2013年度世界最经固体材料,可用作处理海上原油泄漏的吸油材料 | |
| B. | 过氧化氢酶、酚醛树脂、尼龙、有机玻璃、PVC都是高分子化合物 | |
| C. | 生物炼铜的原理是利用某些具有特殊本领的细菌把不溶性的硫化铜转化为铜单质 | |
| D. | 电解熔融氧化铝、粗硅的制取涉及化学变化,煤焦油中提取苯是物理变化 |
10.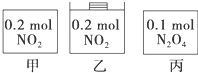 甲、乙、丙三个容器中最初存在的物质及数量如图所示,三个容器最初的容积相等,温度相同,反应中甲、丙的容积不变,乙中的压强不变,在一定温度下反应达到平衡.下列说法正确的( )
甲、乙、丙三个容器中最初存在的物质及数量如图所示,三个容器最初的容积相等,温度相同,反应中甲、丙的容积不变,乙中的压强不变,在一定温度下反应达到平衡.下列说法正确的( )
 甲、乙、丙三个容器中最初存在的物质及数量如图所示,三个容器最初的容积相等,温度相同,反应中甲、丙的容积不变,乙中的压强不变,在一定温度下反应达到平衡.下列说法正确的( )
甲、乙、丙三个容器中最初存在的物质及数量如图所示,三个容器最初的容积相等,温度相同,反应中甲、丙的容积不变,乙中的压强不变,在一定温度下反应达到平衡.下列说法正确的( )| A. | 平衡时各容器内n(NO2)的大小顺序为乙>甲>丙 | |
| B. | 平衡时NO2的百分含量:乙>甲=丙 | |
| C. | 平衡时甲中NO2与丙中N2O4的转化率一定相同 | |
| D. | 平衡时混合物的平均相对分子质量:乙>甲=丙 |
9.电离平衡常数是衡量弱电解质电离程度的量.已知如下表数据(25℃):
(1)25℃时,等浓度的三种溶液(A.NaCN溶液、B.Na2CO3溶液、C.CH3COONa溶液)的pH由大到小的顺序为b>a>c.(填写序号)
(2)25℃时,向NaCN溶液中通入少量CO2,所发生反应的化学方程式为NaCN+CO2+H2O=NaHCO3+HCN.
(3)现有浓度为0.02mol/L的HCN与0.01mol/L NaOH等体积混合后,测得c(Na+)>c(CN-),下列关系正确的是BD.
A.c(H+)>c(OH-)
B.c(H+)<c(OH-)
C.c(H+)+c(HCN)=c(OH-)
D.c(HCN)+c(CN-)=0.01mol/L
(4)浓的Al2(SO4)3溶液和浓的小苏打(NaHCO3)溶液混合可用于灭火,请用离子反应方程式表示灭火的原理Al3++3HCO3-=Al(OH)3↓+3CO2↑.
(5)已知NaHC2O4水溶液显酸性,请写出该溶液中各离子浓度的大小c(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-).
| 化学式 | 电离平衡常数 |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.4×10-7,K2=4.7×10-11 |
(2)25℃时,向NaCN溶液中通入少量CO2,所发生反应的化学方程式为NaCN+CO2+H2O=NaHCO3+HCN.
(3)现有浓度为0.02mol/L的HCN与0.01mol/L NaOH等体积混合后,测得c(Na+)>c(CN-),下列关系正确的是BD.
A.c(H+)>c(OH-)
B.c(H+)<c(OH-)
C.c(H+)+c(HCN)=c(OH-)
D.c(HCN)+c(CN-)=0.01mol/L
(4)浓的Al2(SO4)3溶液和浓的小苏打(NaHCO3)溶液混合可用于灭火,请用离子反应方程式表示灭火的原理Al3++3HCO3-=Al(OH)3↓+3CO2↑.
(5)已知NaHC2O4水溶液显酸性,请写出该溶液中各离子浓度的大小c(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-).
7.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 0.1molCl2常温下与过量NaOH溶液反应转移电子总数为 0.1NA | |
| B. | 25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| C. | 0.25 mol Na2O2中含有的阴离子数为0.5 NA | |
| D. | 1L 0.1mol•L-1的硫化钠溶液中硫离子数目为0.1NA |
6.下列各组物质的分类正确的是( )
①混合物:水玻璃、水银、水煤气
②电解质:明矾、冰醋酸、石膏;
③酸性氧化物:CO2、CO、SO3
④同位素:1H、2H2、3H
⑤同素异形体:C60、金刚石、石墨
⑥干冰、液氯都是非电解质.
①混合物:水玻璃、水银、水煤气
②电解质:明矾、冰醋酸、石膏;
③酸性氧化物:CO2、CO、SO3
④同位素:1H、2H2、3H
⑤同素异形体:C60、金刚石、石墨
⑥干冰、液氯都是非电解质.
| A. | ②⑤ | B. | ②⑤⑥ | C. | ②④⑤⑥ | D. | ①②③④⑤⑥ |
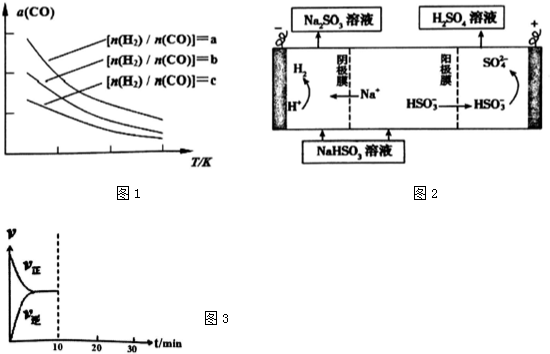
5.图Ⅰ、Ⅱ分别是甲、乙两组同学将反应AsO43-+2I-+2H+═AsO33-+I2+H2O设计成的原电池装置,其中C1、C2均为碳棒.甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40%NaOH溶液.
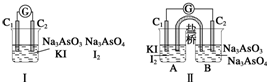
下列叙述正确的是( )

下列叙述正确的是( )
| A. | 甲组操作时,微安表指针不发生偏转 | |
| B. | 甲组操作时,溶液颜色不变 | |
| C. | 乙组操作时,C2作正极 | |
| D. | 乙组操作时,C1上发生的电极反应式为I2+2e-═2I- |
4.标准状况下VL氨气溶解在1L水中,所得溶液的密度为ρ g/ml,质量分数为ω,物质浓度为c mol/L,则下列关系中正确的是( )
| A. | c=$\frac{Vρ}{17V+22400}$ | B. | ω=$\frac{17c}{100ρ}$ | ||
| C. | ω=$\frac{17V}{17V+22400}$ | D. | ρ=$\frac{17V+22400}{22.4+22.4V}$ |
3.下列说法错误的为( )
0 160926 160934 160940 160944 160950 160952 160956 160962 160964 160970 160976 160980 160982 160986 160992 160994 161000 161004 161006 161010 161012 161016 161018 161020 161021 161022 161024 161025 161026 161028 161030 161034 161036 161040 161042 161046 161052 161054 161060 161064 161066 161070 161076 161082 161084 161090 161094 161096 161102 161106 161112 161120 203614
| A. | 从1L、1mol/L NaCl溶液中取出10mLNaCl溶液,其浓度仍为1mol/L | |
| B. | 配制0.5L、10mol/L的盐酸,需要氯化氢气体112升(标况) | |
| C. | 0.5L、2mol/L BaCl2溶液中Ba2+ 和 Cl-的总个数约为3×6.02×1023 | |
| D. | 10g、98%的浓硫酸(密度为1.84g/cm3 )与10mL、1.84mol/L的浓硫酸浓度不同 |