7.NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 2.3 g Na变成Na+时,失去的电子数为0.2NA | |
| B. | 0.2NA个H2SO4与19.6 g H3PO4含有相同的氧原子数 | |
| C. | 28 g N2与CO的混合气体,所含的原子数为NA | |
| D. | 含有NA个氧原子的H2SO4的物质的量是4 mol |
6.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 12g石墨烯(单层石墨)中含C原子个数为NA | |
| B. | 等质量的C18O与NO含有的原子个数均为2NA | |
| C. | 1.0L 1.0mol•L-1的NaAlO2水溶液中含有的氧原子数为2NA | |
| D. | 25℃时1L pH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA |
4.已知H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)↓+2H2O(l)△H=-1 584.2kJ•mol-1;HCl(aq)与NaOH(aq)反应的中和热△H=-55.6kJ•mol-1.则生成SO42-(aq)+Ba2+(aq)=BaSO4(s)的反应热等于( )
| A. | -1 528.6 kJ•mol-1 | B. | -1 473 kJ•mol-1 | ||
| C. | +1 473 kJ•mol-1 | D. | +1 528.6 kJ•mol-1 |
2.下列有机物不能以苯为原料一步制取的是( )
| A. |  | B. |  | C. |  | D. |  |
1.下列实验室制气体的措施或方法中主要利用的是原电池反应原理的是( )
| A. | 实验室制H2时,向Zn和稀硫酸反应体系中加入少量的CuSO4固体 | |
| B. | 实验室制O2时,向H2O2溶液中加入少量的MnO2 | |
| C. | 实验室制CO2时,用盐酸和CaCO3反应 | |
| D. | 实验室制NH3时,加热Ca(OH)2和NH4Cl和混合物 |
5.设阿伏加德罗常数的值为NA,下列说法正确的是( )
| A. | 3.1 g由白磷和红磷组成的混合物中含有磷原子的数目为0.1NA | |
| B. | 0.1mol${\;}_{35}^{81}$Br原子中含中子数为3.5NA | |
| C. | 标准状况下,11.2LCHCl3中含有C-Cl键的数目为1.5NA | |
| D. | 0.5L1.0mol•L-1NH4Al(SO4)2溶液中含有的NH${\;}_{4}^{+}$数目为0.5NA |
4.某新型燃料电池以乙烯为原料制备乙醛并获得电能,工作原理如图所示.下列有关说法正确的是( )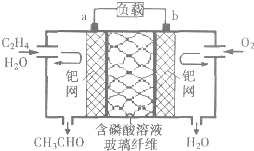

| A. | a电极为正电极 | |
| B. | 放电时,若有2mol电子转移,则理论上需要消耗28g乙烯 | |
| C. | a极的电极反应式为CH2═CH2+2OH--2e-═CH3CHO+H2O | |
| D. | 电子移动方向:a电极→磷酸溶液→b电极 |
3.表是生活生产中常见的物质,表中列出了它们的一种主要成分(其它成分未列出)
(1)请你对表中①~⑦的主要成分进行分类(填编号)属于盐的是①③,属于电解质的是①②③⑦,属于非电解质的是④⑥.
(2)写出②与⑦反应的离子方程式CH3COOH+OH-=CH3COO-+H2O.少量盐酸与③反应的离子方程式为CO32-+H+=HCO3-.
0 160909 160917 160923 160927 160933 160935 160939 160945 160947 160953 160959 160963 160965 160969 160975 160977 160983 160987 160989 160993 160995 160999 161001 161003 161004 161005 161007 161008 161009 161011 161013 161017 161019 161023 161025 161029 161035 161037 161043 161047 161049 161053 161059 161065 161067 161073 161077 161079 161085 161089 161095 161103 203614
| 编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 名称 | 绿矾 | 醋精 | 苏打 | 酒精 | 铜导线 | 蔗糖 | 烧碱 |
| 主要成分 | FeSO4 | CH3COOH | Na2CO3 | CH3CH2OH | Cu | C12H22O11 | NaOH |
(2)写出②与⑦反应的离子方程式CH3COOH+OH-=CH3COO-+H2O.少量盐酸与③反应的离子方程式为CO32-+H+=HCO3-.
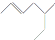 :5-甲基-2-庚烯,
:5-甲基-2-庚烯,