2.一定条件下将2mol SO2和2mol SO3气体混合于一固定容积的密闭容器中,发生反应:2SO2+O2?2SO3,平衡时SO3为n mol,在相同温度下,分别按下列配比在上述容器中放入起始物质,平衡时SO3的物质的量可能大于n的是( )
| A. | 2molSO2+1molO2 | B. | 2molSO2+1molO2+2molSO3 | ||
| C. | 4molSO2+1molO2 | D. | 3molSO2+0.5molO2+1molSO3 |
1.若将基态P原子的电子排布式写成1s22s22p63s23px23py1,它违背了( )
| A. | 泡利原理 | B. | 能量守恒原理 | C. | 构造原理 | D. | 洪特规则 |
20.臭氧具有优异的杀菌、消毒功能.许多臭氧消毒柜通过电击空气中的氧气生成臭氧,在该过程中,电的作用是( )
| A. | 氧化 | B. | 还原 | C. | 催化 | D. | 提供能量 |
19.我国具有独立知识产权的电脑芯片“龙芯一号”的问世,填补了我国计算机制造史上的一项空白.下列对晶体硅的有关叙述正确的是( )
| A. | 晶体硅和金刚石的物理性质相似 | |
| B. | 硅在地壳中含量居第二位,可以以游离态存在于自然界中 | |
| C. | 晶体硅是一种良好的半导体材料,但是它提炼工艺复杂,价格昂贵 | |
| D. | 晶体硅具有金属光泽,故它属于金属材料,可以导电 |
18.氧化还原反应是一类重要的化学反应,广泛存在于自然界中,对人们的生产、生活有着十分重要的作用.你认为下列对氧化还原反应的描述不正确的是( )
| A. | 肯定有电子得失 | |
| B. | 肯定是有关氧元素的反应 | |
| C. | 肯定有化合价的变化 | |
| D. | 氧化剂得到电子总数与还原剂失去电子总数相等 |
17.设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 常温下,500mL 2mol•L-1的Na2CO3溶液中含Na+数目为NA | |
| B. | 常温下,2.7g铝与足量盐酸反应,失去电子数为0.3NA | |
| C. | 1.8gNH4+的离子中含有的质子数为0.1NA | |
| D. | 标准状况下,1 L水所含分子数为$\frac{1}{22.4}$NA |
16.设 NA 为阿伏加德罗常数,下列说法正确的是( )
| A. | 1 mol 氧单质一定含有 2 NA 个氧原子 | |
| B. | 含 4 mol Si-O 键的石英晶体中含氧原子数为 4 NA | |
| C. | 6.8 g 液态 KHSO4中含有 0.05 NA 个阳离子 | |
| D. | 1 mol H3O+中含质子数为 10 NA |
13.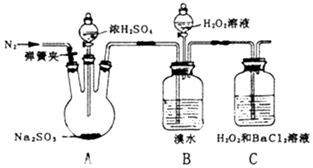 为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验).
为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验).
(1)A中发生反应的化学方程式是Na2SO3(固)+H2SO4(浓)=Na2SO4+SO2↑+H2O.
(2)甲同学通过C中产生白色沉淀,得出结论,氧化性:H2O2>SO2.
①乙同学认为不能得出此结论,认为在滴加浓硫酸之前应增加一步操作,该操作是打开弹簧夹,通入N2,待排净装置内空气后,关闭弹簧夹.
②丙同学认为还应该在B和C之间增加洗气瓶D,D中盛放的试剂是CCl4或苯或饱和NaHSO3溶液.
(3)iii中滴入少量H2O2没有明显变化.提出假设:
观点1:H2O2的量少不能氧化Br-
观点2:B中有未反应的H2SO3
为验证观点2,应进行的实验操作及现象是取少量滴加H2O2溶液前的B中溶液于试管中,加热,将气体通入品红溶液中,品红溶液褪色.
(4)通过上述全部实验,得出结论:H2O2、SO2、Br2氧化性由强到弱的顺序是H2O2>Br2>SO2.
0 160900 160908 160914 160918 160924 160926 160930 160936 160938 160944 160950 160954 160956 160960 160966 160968 160974 160978 160980 160984 160986 160990 160992 160994 160995 160996 160998 160999 161000 161002 161004 161008 161010 161014 161016 161020 161026 161028 161034 161038 161040 161044 161050 161056 161058 161064 161068 161070 161076 161080 161086 161094 203614
 为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验).
为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验).| 实验操作 | 实验现象 |
| i.打开A中分液漏斗活塞,滴加浓硫酸 | A中有气泡产生,B中红棕色溴水褪色,C中有白色沉淀 |
| ii.取C中沉淀加入盐酸 | C中白色沉淀不溶解 |
| iii.打开B中分液漏斗活塞,逐滴滴加H2O2 | 开始时颜色无明显变化,继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
(2)甲同学通过C中产生白色沉淀,得出结论,氧化性:H2O2>SO2.
①乙同学认为不能得出此结论,认为在滴加浓硫酸之前应增加一步操作,该操作是打开弹簧夹,通入N2,待排净装置内空气后,关闭弹簧夹.
②丙同学认为还应该在B和C之间增加洗气瓶D,D中盛放的试剂是CCl4或苯或饱和NaHSO3溶液.
(3)iii中滴入少量H2O2没有明显变化.提出假设:
观点1:H2O2的量少不能氧化Br-
观点2:B中有未反应的H2SO3
为验证观点2,应进行的实验操作及现象是取少量滴加H2O2溶液前的B中溶液于试管中,加热,将气体通入品红溶液中,品红溶液褪色.
(4)通过上述全部实验,得出结论:H2O2、SO2、Br2氧化性由强到弱的顺序是H2O2>Br2>SO2.