题目内容
1.若将基态P原子的电子排布式写成1s22s22p63s23px23py1,它违背了( )| A. | 泡利原理 | B. | 能量守恒原理 | C. | 构造原理 | D. | 洪特规则 |
分析 能量最低原理:原子核外电子先占有能量低的轨道,然后依次进入能量高的轨道;
泡利不相容原理:每个原子轨道上最多只能容纳2个自旋状态相反的电子;
洪特规则:洪特规则是在等价轨道(相同电子层、电子亚层上的各个轨道)上排布的电子将尽可能分占不同的轨道,且自旋方向相同.
解答 解:P原子3p能级上有3个轨道,3p能级上有3个电子,3个电子应该排在3个不同的轨道上,且自旋方向相同,若将P原子的电子排布式写成1s22s22p63s23px23py1,它违背了洪特规则,
故选D.
点评 本题考查了原子结构构造原理,明确这几个概念是解本题关键,难度不大.

练习册系列答案
相关题目
20.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,11.2 L CCl4中含有的C Cl键的个数为2NA | |
| B. | 1 mol Na2O和Na2O2中含有的阴、阳离子总数是3 NA | |
| C. | 常温下,0.1 mol Cl2通入NaOH溶液中充分反应,转移电子数为0.2 NA | |
| D. | 1 L 0.1 mol•L-1氨水溶液中所含的离子和分子总数大于0.1 NA但小于0.2 NA |
1.表中陈述I、II均正确,且两者在反应原理上相似的是( )
| 选项 | 陈述I | 陈述II |
| A | 向酚酞溶液中加Na2O2,溶液先变红后褪色 | 向石蕊溶液中通入SO2,溶液先变红后褪色 |
| B | 将SO2和Cl2同时通入BaCl2溶液中,产生白色沉淀 | 将CO2和NH3同时通入CaCl2溶液中,产生白色沉淀 |
| C | 向MgCl2溶液中加入NaOH溶液生成白色沉淀 | 向FeCl3溶液中加入NaOH溶液生成红褐色沉淀 |
| D | Na投入水中产生大量气泡 | Na2CO3投入盐酸中产生大量气泡 |
| A. | A | B. | B | C. | C | D. | D |
9.关于化学反应与能量的说法正确的是( )
| A. | 化学键断裂需要吸收能量 | |
| B. | 化学反应中能量变化的大小与反应物的质量多少无关 | |
| C. | 在化学反应过程中反应物的总能量总是等于生成物的总能量 | |
| D. | 放热反应都能自发进行,吸热反应需要在加热的条件下才能进行 |
16.设 NA 为阿伏加德罗常数,下列说法正确的是( )
| A. | 1 mol 氧单质一定含有 2 NA 个氧原子 | |
| B. | 含 4 mol Si-O 键的石英晶体中含氧原子数为 4 NA | |
| C. | 6.8 g 液态 KHSO4中含有 0.05 NA 个阳离子 | |
| D. | 1 mol H3O+中含质子数为 10 NA |
6.下列分类依据和结论都正确的是( )
| A. | HClO、浓硫酸、HNO3均具有氧化性,都是氧化性酸 | |
| B. | H2O、Na2O2、HClO均含有氧元素,都是氧化物 | |
| C. | HF、NH3、CH3CH2OH都易溶于水,都是电解质 | |
| D. | 碱性氧化物都是金属氧化物,因此金属氧化物都是碱性氧化物 |
13.下列物质能使干燥的蓝色石蕊试纸先变红后褪色的是( )
①氯气;②液氯;③新制氯水;④亚硫酸溶液;⑤盐酸酸化的漂白粉溶液.
①氯气;②液氯;③新制氯水;④亚硫酸溶液;⑤盐酸酸化的漂白粉溶液.
| A. | ①②③ | B. | ①②③⑤ | C. | ③⑤ | D. | ③④⑤ |
10.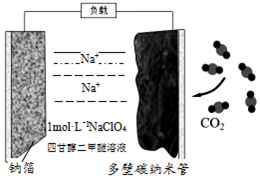 最近我国科学家发明“可充电钠-二氧化碳电池”(如图),放电时电池总反应为:a+3CO2=2Na2CO3+C.下列说法错误的是( )
最近我国科学家发明“可充电钠-二氧化碳电池”(如图),放电时电池总反应为:a+3CO2=2Na2CO3+C.下列说法错误的是( )
 最近我国科学家发明“可充电钠-二氧化碳电池”(如图),放电时电池总反应为:a+3CO2=2Na2CO3+C.下列说法错误的是( )
最近我国科学家发明“可充电钠-二氧化碳电池”(如图),放电时电池总反应为:a+3CO2=2Na2CO3+C.下列说法错误的是( )| A. | 充电时,钠箔与外接电源的负极相连 | |
| B. | 电池工作温度可能在200℃以上 | |
| C. | 放电时,Na+向正极移动 | |
| D. | 放电时,正极的电极反应为:4Na++3CO2+4e-=2Na2CO3+C |
11.关注营养,促进健康.下列观点不正确的是( )
| A. | 加碘食盐含有碘化钾( KI) | |
| B. | 食醋既是调味剂又是防腐剂 | |
| C. | 坏血病患者应该多吃的食物是水果和蔬菜 | |
| D. | 人体必需的微量元素不都是金属元素 |