11.从矿物学资料查得,一定条件下自然界存在如下反应:14CuSO4+5FeS2+12H2O═7Cu2S+5FeSO4+12H2SO4,下列说法正确的是( )
| A. | CuSO4是氧化剂,FeS2既是氧化剂又是还原剂 | |
| B. | 当生成7molCu2S时,共转移电子14mol | |
| C. | 产物中的SO42-离子全部是氧化产物 | |
| D. | 该反应中氧化剂、还原剂的物质的量之比为14:5 |
10.下列叙述正确的是( )
| A. | 碳族元素都是非金属元素,其非金属性随核电荷数的增加而减弱 | |
| B. | 石英、水晶、硅石的主要成分都是二氧化硅 | |
| C. | 二氧化硅的化学性质活泼,能与任意的酸、碱发生反应 | |
| D. | 碳族元素的单质都有导电性 |
9.下列有关NaClO和NaCl混合溶液的叙述错误的是( )
| A. | 该溶液可做杀菌消毒剂和漂白剂 | |
| B. | 该溶液中,OH-、K+、SO42-、NO3-可以大量共存 | |
| C. | 向该溶液中滴入少量FeSO4溶液,反应的离子方程式为2Fe2++ClO-+2H+═Cl-+2Fe3++H2O | |
| D. | 向该溶液中加入浓盐酸,每产生1 mol Cl2,转移电子约为6.02×1023个 |
8.中学化学实验中应用最广泛的仪器之一是滴瓶.滴瓶用于盛放各种溶液,关于滴瓶中滴管的使用,叙述不正确的是( )
| A. | 向试管中滴加溶液时,滴管尖嘴不能伸入试管口内 | |
| B. | 不能将滴管水平拿持 | |
| C. | 加完药品后应将滴管洗净后再放回原瓶 | |
| D. | 滴管除了原滴瓶外,不能放在别的地方 |
6.下列叙述不正确的是( )
| A. | 1 mol H2约含有6.02×1023个氢分子 | |
| B. | 1 mol H2O的质量为18 g | |
| C. | 1 mol O2的体积为22.4 L | |
| D. | 1L 1 mol/L NaCl溶液中含1 molNa+ |
5.已知:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1=-890.3kJ•mol-1;
H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H2=-285.8kJ•mol-1.
CO2与H2反应生成甲烷气体与液态水的热化学方程式为CO2(g)+4H2(g)═CH4(g)+2H2O(l)△H3,则△H3为( )
H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H2=-285.8kJ•mol-1.
CO2与H2反应生成甲烷气体与液态水的热化学方程式为CO2(g)+4H2(g)═CH4(g)+2H2O(l)△H3,则△H3为( )
| A. | -252.9 kJ•mol-1 | B. | +252.9 kJ•mol-1 | C. | -604.5 kJ•mol-1 | D. | +604.5 kJ•mol-1 |
3.设NA为阿伏伽德罗常数,下列叙述正确的是( )
| A. | 2.4g镁的原子核外电子数为0.2NA | |
| B. | 2.3 g Na与氧气反应生成Na2O和Na2O2,转移电子数为0.1NA | |
| C. | 1mol丙烷分子中11 mol共价键 | |
| D. | 1.4 g C2H4和C3H6的混合气体中,含0.2NA的C原子 |
2.用一质量为1.2g的铝片与45mL 4mol/L稀硫酸反应制取H2,若要增大反应速率,采取的措施:①再加入20mL 4mol/L硫酸;②改用30mL 6mol/L的稀硫酸;③改用20mL 18mol/L浓硫酸;④改用1.2g铝粉代替1.2g铝片;⑤适当升高温度;⑥在敞口容器中反应.其中正确的是( )
0 160886 160894 160900 160904 160910 160912 160916 160922 160924 160930 160936 160940 160942 160946 160952 160954 160960 160964 160966 160970 160972 160976 160978 160980 160981 160982 160984 160985 160986 160988 160990 160994 160996 161000 161002 161006 161012 161014 161020 161024 161026 161030 161036 161042 161044 161050 161054 161056 161062 161066 161072 161080 203614
| A. | ①②③④ | B. | ②④⑤ | C. | ②③④⑤ | D. | ②③④⑤⑥ |
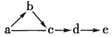 其中:a是单质,b是气体,c、d是氧化物,e是最高价氧化物对应的水化物.
其中:a是单质,b是气体,c、d是氧化物,e是最高价氧化物对应的水化物.