题目内容
2.用一质量为1.2g的铝片与45mL 4mol/L稀硫酸反应制取H2,若要增大反应速率,采取的措施:①再加入20mL 4mol/L硫酸;②改用30mL 6mol/L的稀硫酸;③改用20mL 18mol/L浓硫酸;④改用1.2g铝粉代替1.2g铝片;⑤适当升高温度;⑥在敞口容器中反应.其中正确的是( )| A. | ①②③④ | B. | ②④⑤ | C. | ②③④⑤ | D. | ②③④⑤⑥ |
分析 增大反应速率,可增大固体表面积、升高温度,增大浓度,加入催化剂或形成原电池反应等,以此解答该题.
解答 解:①再加入20mL 4mol/L硫酸,硫酸浓度不变,反应速率不变,故错误;
②改用30mL 6mol/L的稀硫酸,硫酸浓度增大,反应速率增大,故正确;
③改用20mL 18mol/L浓硫酸,与铝在常温下发生钝化反应,不生成氢气,故错误;
④改用1.2g铝粉代替1.2g铝片,固体表面积增大,反应速率增大,故正确;
⑤适当升高温度,活化分子百分数增大,反应速率增大,故正确;
⑥在敞口容器中反应,反应物浓度不变,不影响反应速率,故错误.
故选B.
点评 本题考查反应速率的影响因素,为高频考点,侧重于学生的分析能力和基本理论知识的理解和运用的考查,注意相关基础知识的积累,把握影响反应速率的因素和影响原因,难度不大.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
13.下列实验操作正确的是( )
| A. |  读取液体体积 | B. |  液体的倾倒 | C. | 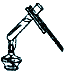 液体加热 | D. |  |
10.NA代表阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,22.4LCl2与足量的铁粉反应,转移的电子数为3NA | |
| B. | 含23g钠元素的Na2O和Na2O2混合物中阴离子数目介于0.5NA和NA之间 | |
| C. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$4N2↑+2HNO3+9H2O中氧化产物比还原产物每多14g,转移电子数为15NA | |
| D. | 在0℃、101kPa条件下,11.2L丁烷中含极性共价键数目为5NA |
17.已知某溶液中c(Na+)=0.2mol/L,c(Mg2+)=0.25mol/L,c(Cl-)=0.4mol/L,如果溶液中还有SO42-,那么c(SO42-)应为( )
| A. | 0.1 mol/L | B. | 0.3 mol/L | C. | 0.15 mol/L | D. | 0.5 mol/L |
14.提纯少量含碳酸氢钠杂质的碳酸钠固体所需用的仪器是( )
①试管;②泥三角;③蒸发皿;④试管夹;⑤坩埚;⑥玻璃棒;⑦石棉网;⑧坩埚钳.
①试管;②泥三角;③蒸发皿;④试管夹;⑤坩埚;⑥玻璃棒;⑦石棉网;⑧坩埚钳.
| A. | ①④ | B. | ②⑤⑧ | C. | ③⑥ | D. | ⑥⑦ |
11.1gN2中含有n个N原子,则阿伏伽德罗常数NA可以表示为( )
| A. | 14nmol-1 | B. | 28nmol-1 | C. | $\frac{n}{14}$mo l-1 | D. | $\frac{n}{28}$mol-1 |
12.下列物质中,属于酚类的是( )
| A. | 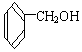 | B. | 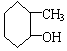 | C. | 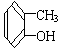 | D. | 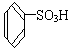 |