17.常温下,wg某硝酸盐(摩尔质量为Mg•mol-1)溶于VmL水(ρ=1g•mL-1)中恰好达到饱和,该饱和溶液的密度为ag•cm-3.下列关系式不正确的是( )
| A. | ω=$\frac{w}{w+V}$×100% | B. | S=$\frac{w}{V}$×100g | ||
| C. | c=$\frac{1000w}{MV}$mol•L-1 | D. | c=$\frac{1000aw}{M(w+V)}$mol•L-1 |
16.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 20gD2O含有的质子数为10NA | |
| B. | 1molNa2O2与足量水反应转移的电子数为NA,生成的气体的标况下的体积为22.4L | |
| C. | 1L0.1mol/LHF溶液中含有共价键数目为0.1NA | |
| D. | NA个Fe(OH)3胶体粒子的质量为107g |
15.水溶液中能大量共存的一组离子是( )
| A. | Na+、Ca2+、Cl-、SO42- | B. | Al3+、Na+、SO32-、HCO3- | ||
| C. | Mg2+、NH4+、Cl-、SO42- | D. | K+、Fe3+、NO3-、OH- |
13.一定温度下,在恒容密闭容器中发生可逆反应N2+3H2?2NH3,已知某时刻存在N2、H2、NH3的浓度为1mol•L-1、2mol•L-1、2mol•L-1,当达到平衡状态可能存在的数据是( )
| A. | N2为$\frac{1}{3}$mol•L-1 | B. | NH3为$\frac{10}{3}$mol•L-1 | ||
| C. | H2为5.5mol•L-1 | D. | N2为1.5mol•L-1,H2为3.5mol•L-1 |
12.下列有关0.1mol•L-1 CuSO4溶液的说法正确的是( )
| A. | 该溶液中SO42-的浓度为0.1mol•L-1 | |
| B. | 该溶液中SO42-的物质的量为0.1mol | |
| C. | 与16.0gCuSO4溶于1L水中所得溶液的浓度相等 | |
| D. | 与16.0gCuSO4•5H2O溶于水中,然后稀释至1L所得溶液的浓度相等 |
11.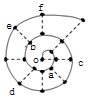 同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个弧线上的“•”代表一种元素,其中O点代表氢元素.下列说法中错误的是( )
同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个弧线上的“•”代表一种元素,其中O点代表氢元素.下列说法中错误的是( )
 同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个弧线上的“•”代表一种元素,其中O点代表氢元素.下列说法中错误的是( )
同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个弧线上的“•”代表一种元素,其中O点代表氢元素.下列说法中错误的是( )| A. | 最高价氧化物对应的水化物的碱性:c<a | |
| B. | 简单离子半径:c>e>b | |
| C. | 简单离子影响水的电离能力:e>a>f | |
| D. | 单质的熔点:c>d>e |
9.下列图示正确的是( )
0 160700 160708 160714 160718 160724 160726 160730 160736 160738 160744 160750 160754 160756 160760 160766 160768 160774 160778 160780 160784 160786 160790 160792 160794 160795 160796 160798 160799 160800 160802 160804 160808 160810 160814 160816 160820 160826 160828 160834 160838 160840 160844 160850 160856 160858 160864 160868 160870 160876 160880 160886 160894 203614
| A. | 水合氢离子: | B. | 氢氧根: | C. | 水合钠离子: | D. | 水合氯离子: |
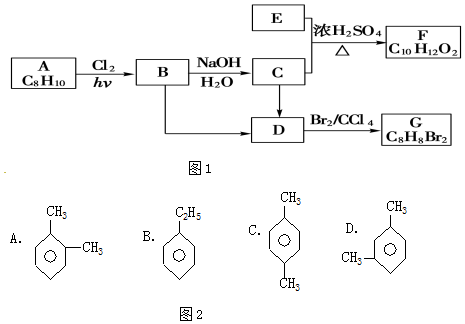
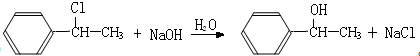 ;
; ;
;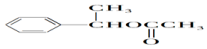 ;
; (结构简式).
(结构简式).