15.下列有关性质的比较,错误的是( )
| A. | 酸性:H2SO4>H3PO4 | B. | 非金属性:Cl>Br | ||
| C. | 碱性:NaOH>Mg(OH)2 | D. | 熔点:K>Na |
14.下列物质的性质可以用“键能”来解释的是( )
| A. | SiO2熔点高 | B. | 氩气性质稳定 | C. | 碘易升华 | D. | NH3极易溶于水 |
13.许多国家重视海水资源的综合利用,不需要化学变化就能够从海水中获得的物质是( )
| A. | 氯、溴、碘 | B. | 烧碱、氢气 | C. | 粗盐、淡水 | D. | 钠、镁、铝 |
12.下列表示正确的是( )
| A. | CH4的比例模型 | B. | 二氧化碳的结构式 O-C-O | ||
| C. | S2-的结构示意图 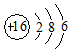 | D. | 氯化钠的电子式  |
10.硅元素的化合物有多种.
回答下列问题:
(1)SiH4的沸点比CH4高,原因是二者是结构相似的分子晶体,SiH4的分子量比CH4的分子量大,范德华力大,所以沸点比CH4高.
(2)硅与碳同主族,也有系列氢化物,但硅院在种类和数量上都远不如烷烃多.根据下表中所列键能数据,简要分析可能的原因Si-Si的键能比C-C小,Si-H的键能也比C-H小,更容易断裂,所以硅烷的种类和数量都比烷烃少.
氮化硅(Si3N4)是一种重要的陶瓷材料,可用石英与焦炭在800℃的氮气气氛下合成:
3SiO2(s)+6C(s)+2N2(g) $\stackrel{高温}{?}$Si3N4(s)+6CO(g)
(3)标出上述反应中电子转移的数目和方向.
(4)该反应的平衡常数表达式K=$\frac{{C}^{6}(CO)}{C({N}_{2})}$.已知平衡常数:K(800℃)>K(850℃),则反 应是放热反应(填“放热”或“吸热”).
(5)任写两种能提高二氧化硅转化率的措施降温、减小压强.
(6)一定温度下,在2L密闭容器内,充入一定量的反应物,5分钟时达到平衡,测得容器内气体增加了0.4mol,用CO表示该反应时间内的反应速率为0.06mol/(L•min).
回答下列问题:
(1)SiH4的沸点比CH4高,原因是二者是结构相似的分子晶体,SiH4的分子量比CH4的分子量大,范德华力大,所以沸点比CH4高.
(2)硅与碳同主族,也有系列氢化物,但硅院在种类和数量上都远不如烷烃多.根据下表中所列键能数据,简要分析可能的原因Si-Si的键能比C-C小,Si-H的键能也比C-H小,更容易断裂,所以硅烷的种类和数量都比烷烃少.
| 化学键 | C-C | C-H | Si-Si | Si-H |
| 键能/(kJ•mol-1) | 356 | 413 | 226 | 318 |
3SiO2(s)+6C(s)+2N2(g) $\stackrel{高温}{?}$Si3N4(s)+6CO(g)
(3)标出上述反应中电子转移的数目和方向.
(4)该反应的平衡常数表达式K=$\frac{{C}^{6}(CO)}{C({N}_{2})}$.已知平衡常数:K(800℃)>K(850℃),则反 应是放热反应(填“放热”或“吸热”).
(5)任写两种能提高二氧化硅转化率的措施降温、减小压强.
(6)一定温度下,在2L密闭容器内,充入一定量的反应物,5分钟时达到平衡,测得容器内气体增加了0.4mol,用CO表示该反应时间内的反应速率为0.06mol/(L•min).
8.25℃时,将两种不同浓度的某一元酸HA分别与NaOH溶液等体积混合(混合后溶液体积等于混合前两溶液体积之和),测得反应后溶液的pH如表所示.下列判断错误的是( )
| 实验编号 | 起始浓度 (mol/L) | 反应后溶液的pH | |
| C(HA) | C(NaOH) | ||
| ① | 0.10 | 0.10 | 9 |
| ② | x | 0.05 | 7 |
| A. | HA是弱酸 | |
| B. | x>0.05 | |
| C. | 实验①所得溶液中:c(A-)+c(HA)=0.10mol/L | |
| D. | 实验②所得溶液中:c(Na+)=c(A-) |
7.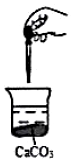 如图,向烧杯中滴加几滴浓盐酸,CaCO3固体还有剩余(忽略体积、温度的变化),下列数值变小的是( )
如图,向烧杯中滴加几滴浓盐酸,CaCO3固体还有剩余(忽略体积、温度的变化),下列数值变小的是( )
 如图,向烧杯中滴加几滴浓盐酸,CaCO3固体还有剩余(忽略体积、温度的变化),下列数值变小的是( )
如图,向烧杯中滴加几滴浓盐酸,CaCO3固体还有剩余(忽略体积、温度的变化),下列数值变小的是( )| A. | c(Ca2+) | B. | c(CO32-) | C. | c(H+) | D. | c(碳酸钙的溶解度) |
6.已知反应:3C12+NH3→6NH4Cl+N2,下列分析正确的是(设阿伏伽德罗常数为NA)( )
0 160664 160672 160678 160682 160688 160690 160694 160700 160702 160708 160714 160718 160720 160724 160730 160732 160738 160742 160744 160748 160750 160754 160756 160758 160759 160760 160762 160763 160764 160766 160768 160772 160774 160778 160780 160784 160790 160792 160798 160802 160804 160808 160814 160820 160822 160828 160832 160834 160840 160844 160850 160858 203614
| A. | 若3molC12反应,得到氧化产物6mol | |
| B. | 若常温下生成22.4LN2,转移电子数6NA | |
| C. | 若转移6mol电子,被氧化的NH3是8mol | |
| D. | 若生成1 molNH4Cl转移电子n个,则NA=n |

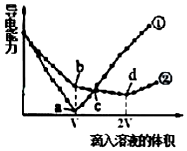 镁、钡是位于同一主族的活泼的金属元素.
镁、钡是位于同一主族的活泼的金属元素. .
.