题目内容
7.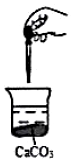 如图,向烧杯中滴加几滴浓盐酸,CaCO3固体还有剩余(忽略体积、温度的变化),下列数值变小的是( )
如图,向烧杯中滴加几滴浓盐酸,CaCO3固体还有剩余(忽略体积、温度的变化),下列数值变小的是( )| A. | c(Ca2+) | B. | c(CO32-) | C. | c(H+) | D. | c(碳酸钙的溶解度) |
分析 CaCO3固体的溶液中存在溶解平衡:CaCO3(s)?Ca2+(aq)+CO32-(aq),加入少量稀盐酸,发生CO32-+H+=HCO3-或CO32-+2H+=CO2+H2O,平衡正向移动,以此解答该题.
解答 解:CaCO3固体的溶液中存在溶解平衡:CaCO3(s)?Ca2+(aq)+CO32-(aq),加入少量稀盐酸可与CO32-反应促使溶解平衡正向移动,故溶液中c(CO32-)减小,c(Ca2+)及c(H+)增大,c(CaCO3)与温度有关,不变,只有B正确.
故选B.
点评 本题考查难溶电解质的溶解平衡,为高频考点,侧重于学生的分析能力的考查,注意把握物质的性质以及平衡移动的影响因素,题目难度不大.

练习册系列答案
相关题目
18. 常温下,实验测得1.0mol/L NH4HCO3溶液pH=8.0.平衡时碳的分布系数(各含碳微粒的浓度占含碳各种微粒浓度之和的分数)与pH的关系如图所示.下列说法正确的是( )
常温下,实验测得1.0mol/L NH4HCO3溶液pH=8.0.平衡时碳的分布系数(各含碳微粒的浓度占含碳各种微粒浓度之和的分数)与pH的关系如图所示.下列说法正确的是( )
 常温下,实验测得1.0mol/L NH4HCO3溶液pH=8.0.平衡时碳的分布系数(各含碳微粒的浓度占含碳各种微粒浓度之和的分数)与pH的关系如图所示.下列说法正确的是( )
常温下,实验测得1.0mol/L NH4HCO3溶液pH=8.0.平衡时碳的分布系数(各含碳微粒的浓度占含碳各种微粒浓度之和的分数)与pH的关系如图所示.下列说法正确的是( )| A. | 常温下ka(H2CO3)>Kb(NH3•H2O)>Ka2(H2CO3) | |
| B. | pH=13时,溶液中不存在HC03-的水解平衡 | |
| C. | pH由8~11时,$\frac{(C{O}_{3}^{2-})•c({H}^{+})}{c(HC{O}_{3}^{-})}$不变 | |
| D. | pH=3时,有c(NH4+)+c(NH3•H2O)═c(HCO3-)+c(CO32-)+c(H2CO3) |
15.氢氧化钠晶体熔化的过程中,破杯了( )
| A. | 共价键和离子键 | B. | 离子键 | C. | 离子键和金属键 | D. | 共价键 |
2.将足量稀盐酸加到下列固体混合物中,只能发生一种反应的是( )
| A. | NaOH、NaCl、NaAlO2 | B. | KNO3、NaCl、CH3COONa | ||
| C. | Na2S、(NH4)2SO3、AgNO3 | D. | Ba(NO3)2、FeSO4、NH4HCO3 |
12.下列表示正确的是( )
| A. | CH4的比例模型 | B. | 二氧化碳的结构式 O-C-O | ||
| C. | S2-的结构示意图 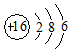 | D. | 氯化钠的电子式  |
19.下列离子方程式正确的是( )
| A. | 金属钠和水反应:Na+2H2O→Na++2OH-+H2↑ | |
| B. | 用氢氧化钠溶液吸收少量二氧化硫气体:SO2+2OH-→SO32-+H2O | |
| C. | 硫酸铵溶液和氢氧化钡溶液反应:Ba2++SO42-→BaSO4↓ | |
| D. | 醋酸和碳酸钙反应:2H++CaCO3→Ca2++CO2↑+H2O |
16.有关实验叙述不正确的是( )
| A. | 滴定管、容量瓶和分液漏斗使用前都要检漏、干燥 | |
| B. | 滴定管没有用标准液润洗,会导致测定结果偏高 | |
| C. | 滴定管中加标准液后,要调节液面位置在零刻度或以下 | |
| D. | 胆矾结晶水含量测定时,需用小火缓慢加热,防止晶体飞溅 |
17.常温下,下列关于pH同为3的盐酸与醋酸两种溶液的说法正确的是( )
| A. | 醋酸溶液的浓度大于盐酸溶液的浓度 | |
| B. | 相同体积的两溶液能中和等物质的量的氢氧化钠 | |
| C. | 两溶液稀释100倍,pH都为5 | |
| D. | 两溶液中分别加入少量对应的钠盐,c(H+) 均明显增大 |