题目内容
9. 镁、钡是位于同一主族的活泼的金属元素.
镁、钡是位于同一主族的活泼的金属元素.回答下列问题:
(1)镁在元素周期表中的位置是:第三周期,第ⅡA族;钡位于周期表第六周期,钡原子最外层电子的电子排布式是:6s2.
(2)铝也是一种活泼金属,铝的金属性比钡的弱(填“强”或“弱”).工业上可用如下方法制取钡:2Al+4BaO$\stackrel{高温}{→}$3Ba↑+BaO•Al2O3,该法制钡的主要原因是c(选填选项)
a.高温时Al的活泼性大于Ba b.高温时BaO•Al2O3比Al2O3稳定
c.Ba的沸点比Al的低 d.高温有利于BaO分解
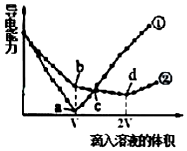
两个烧杯分别盛有VmL、c mol/L的Ba(OH)2溶液,分别向其中滴入c mol/L的H2SO4 和NaHSO4溶液,两烧杯中溶液导电能力随滴入溶液体积的变化分别如图中①、②所示.
(3)写出Ba(OH)2溶液与H2SO4恰好反应的离子方程式:Ba2++2OH-+2H++SO42-=BaSO4↓+H2O.
(4)写出b点溶液中大量存在的阴离子的电子式:
 .
.(5)a、b、c、d点溶液呈中性的是a、d.
分析 (1)镁元素原子核外有12个电子,有三个电子层,最外层2个电子,钡原子位于第ⅡA族最外层电子2个;
(2)常温下Al的金属性比Ba的金属性弱,该反应是利用Ba的沸点比Al的低;
根据图知,a点为Ba(OH)2溶液和H2SO4恰好反应,H2SO4、NaHSO4溶液的物质的量浓度相等,则b点溶液溶质为NaOH,c点,①中稀硫酸过量,溶质为硫酸,②中硫酸氢钠过量,则溶质为NaOH、Na2SO4,d点②中溶质为Na2SO4;
(3)Ba(OH)2溶液与H2SO4恰好反应生成硫酸钡和水;
(4)b点溶液溶质为NaOH,氢氧根离子为阴离子;
(5)a点①中硫酸和氢氧化钡恰好完全反应,溶液中只含水;d点②中溶质为Na2SO4,水和硫酸钠溶液都呈中性,b点溶液溶质为NaOH,c点,①中稀硫酸过量.
解答 解:(1)镁元素原子核外有12个电子,有三个电子层,最外层2个电子,位于第三周期,第ⅡA族,钡位于周期表第六周期,钡原子最外层电子的电子排布式是6s2,
故答案为:第三周期,第ⅡA族;6s2;
(2)利用元素Ba、Al在元素周期表的位置可知金属活泼性:Al<Ba;但Al在高温下可将氧化钡中钡置换出来,原因是Ba的沸点低于铝,高温时Ba转化为气体脱离反应体系,使反应正向进行,
故答案为:弱;c;
(3)Ba(OH)2溶液与H2SO4恰好反应生成硫酸钡和水,反应的离子方程式为:Ba2++2OH-+2H++SO42-=BaSO4↓+H2O,
故答案为:Ba2++2OH-+2H++SO42-=BaSO4↓+H2O;
(4)b点溶液溶质为NaOH,氢氧根离子为阴离子,电子式为: ,故答案为:
,故答案为: ;
;
(5)a点①中硫酸和氢氧化钡恰好完全反应,溶液中只含水;d点②中溶质为Na2SO4,水和硫酸钠溶液都呈中性,b点溶液溶质为NaOH,c点,①中稀硫酸过量,溶质为硫酸,
故答案为:a、d;
点评 本题考查酸碱混合溶液定性判断,为高频考点,侧重考查学生分析判断及识图能力,明确发生的反应及各点溶液中溶质成分是解本题关键,题目难度中等.

 培优三好生系列答案
培优三好生系列答案| A. | Cl2 | B. | KNO3 | C. | SO2 | D. | Al |
| A. | 氧化还原反应 | B. | 置换反应 | C. | 复分解反应 | D. | 分解反应 |
| 元素 | X | Y | Z |
| 最高、最低化合价 | +7 -1 | +6 -2 | +5 -3 |
| A. | 原子序数:X>Y>Z | B. | 原子半径:X>Y>Z | ||
| C. | 稳定性:HX>H2Y>ZH3 | D. | 酸性由强到弱:HXO4>H2YO4>H3ZO4 |
| A. | SiO2熔点高 | B. | 氩气性质稳定 | C. | 碘易升华 | D. | NH3极易溶于水 |
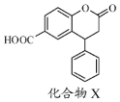
| A. | 分子中两个苯环一定处于同一平面 | |
| B. | 不能与饱和Na2CO3溶液反应 | |
| C. | 1 mol化合物X最多能与2 molNaOH反应 | |
| D. | 在酸性条件下水解,水解产物只有一种 |
| A. | 一定大于7 | B. | 一定等于7 | C. | 一定小于7 | D. | 可能大于7 |
| A. | NaHSO4+NaOH=Na2SO4+H2O | B. | CH3COOH+NaOH→CH3COONa+H2O | ||
| C. | H2SO4+Ba(OH)2→BaSO4↓+2H2O | D. | NH3•H2O+HCl→NH4Cl+H2O |