9.下列说法正确的是( )
| A. | 向装有Fe(NO3)2溶液的试符中加入稀H2SO4,在管口观察到红棕色气体,结论:HNO3分解成了NO2 | |
| B. | 高温下用焦炭还原SiO2制取粗硅 | |
| C. | Na2O2用作呼吸面具的供氧裒剂涉及氧化还原反应 | |
| D. | 浓硝酸有强氧化性,常温下能与Fe发生剧烈反应 |
7.将铁屑溶于过量盐酸后,再加入下列物质:①稀硫酸;②硝酸钠;③氯化铜;④氯水,产生 Fe3+的是( )
| A. | ①④ | B. | ②④ | C. | 只有④ | D. | ①③ |
6.下列描述正确的是( )
| A. | 氨气溶于水能导电,所以氨气是电解质 | |
| B. | 硫粉在过量的纯氧中燃烧可以生成SO2 | |
| C. | 用过量氨水除去Fe3+溶液中的少量Al3+ | |
| D. | 所有铵盐受热均可以分解,产物均有NH3 |
5.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 在强碱性溶液中:Na+、K+、AlO2-、Cu2+ | |
| B. | pH=l的溶液中:HCO3-、NH4+、NO3-、Ca2+ | |
| C. | 无色溶液中:Cu2+、NO3-、Cl-、H+ | |
| D. | 无色溶液中:Na+、K+、ClO-、SO42- |
4.下列指定反应的离子方程式正确的是( )
| A. | Cu 溶于稀 HNO3:Cu+2H++NO3-═Cu2++NO2↑+H2O | |
| B. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 用CH3COOH溶解 CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | FeCl3溶液与Cu反应:2Fe3++Cu═2Fe2++Cu2+ |
3.化学与生活、社会密切相关.下列说法不正确的是( )
| A. | 制备单晶硅的过程中不发生氧化还原反应 | |
| B. | 绚丽缤纷的烟花中添加了含钾,钙,钠,铜等金属元素化合物 | |
| C. | SiO2、NaOH、HF三者两两均能反应 | |
| D. | 氢氧化铝可作胃酸的中和剂 |
2. J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期及中的相对位置如下表;J元素最低负化合价的绝对值与其原子最外层电子数相等:M 是地壳中含虽最多的金属元素.请用化学用语填空..
J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期及中的相对位置如下表;J元素最低负化合价的绝对值与其原子最外层电子数相等:M 是地壳中含虽最多的金属元素.请用化学用语填空..
(1)元素T在周期表中的位置是第三周期、第ⅦA族.
(2)J和氢组成的化合物分子有6个原子,其电子式为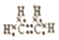 .
.
(3)写出工业冶炼M的化学方程式2Al2O3$\frac{\underline{\;\;\;通电\;\;\;}}{冰晶石}$4Al+3O2↑.
M和R形成的化合物在潮湿的空气中迅速变质,反应的化学方程式为Al2S3+6H2O=2Al(OH)3+3H2S↑.
(4)L的简单单气态氢化物甲的水溶液显碱性.
①在微电子工业中,甲的水溶液可作刻蚀剂H2O2的淸除剂,所发生反应的产物不污染环境,其化学方程式为2NH3•H2O+3H2O2=N2↑+8H2O(或2NH3+3H2O2=N2↑+6H2O).
②一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,.仅改变下表中反应条件M,该平衡体系中随M递增N递减的是AC(选填序号).
③甲和O2组成的混合气共amol导入密闭反应器中,在催化剂存在下发生化学反应.若混合气体中O2为xmol.反应生成的HLO3为ymol.请填表和画出相应的函数图象.
 J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期及中的相对位置如下表;J元素最低负化合价的绝对值与其原子最外层电子数相等:M 是地壳中含虽最多的金属元素.请用化学用语填空..
J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期及中的相对位置如下表;J元素最低负化合价的绝对值与其原子最外层电子数相等:M 是地壳中含虽最多的金属元素.请用化学用语填空..| J | ||||
| R |
(2)J和氢组成的化合物分子有6个原子,其电子式为
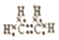 .
.(3)写出工业冶炼M的化学方程式2Al2O3$\frac{\underline{\;\;\;通电\;\;\;}}{冰晶石}$4Al+3O2↑.
M和R形成的化合物在潮湿的空气中迅速变质,反应的化学方程式为Al2S3+6H2O=2Al(OH)3+3H2S↑.
(4)L的简单单气态氢化物甲的水溶液显碱性.
①在微电子工业中,甲的水溶液可作刻蚀剂H2O2的淸除剂,所发生反应的产物不污染环境,其化学方程式为2NH3•H2O+3H2O2=N2↑+8H2O(或2NH3+3H2O2=N2↑+6H2O).
②一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,.仅改变下表中反应条件M,该平衡体系中随M递增N递减的是AC(选填序号).
| 选项 | A | B | C | D |
| M | 温度 | 温度 | H2的物质的量 | 甲的物质的量 |
| N | 甲的物质的量 | 平衡常数K | 甲的转化率 | 生成物总物质的量 |
| 甲转化为HLO3的情况 | X取值范围 | N(HLO3)y/mol |
| 无HLO3的生成 | y=0 | |
| 有部分HLO3的生成 | ||
| 全部生成HLO3 |
1.锂空气电池是一种新型的二次电池,其放电时的工作原理如图所示,下列说法正确的是( )
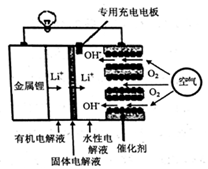

| A. | 正极区产生的LiOH可回收利用 | |
| B. | 电池中的有机电解液可以用稀盐酸代替 | |
| C. | 该电池放电时,正极的反应式为O2+4e-+4H+=2H2O | |
| D. | 该电池充电时,阴极发生了氧化反应:Li++e-=Li |
20.-定温度下,下列溶液的离子浓度关系式正确的是( )
0 160639 160647 160653 160657 160663 160665 160669 160675 160677 160683 160689 160693 160695 160699 160705 160707 160713 160717 160719 160723 160725 160729 160731 160733 160734 160735 160737 160738 160739 160741 160743 160747 160749 160753 160755 160759 160765 160767 160773 160777 160779 160783 160789 160795 160797 160803 160807 160809 160815 160819 160825 160833 203614
| A. | pH=5的 H2S溶液中,c(H+)=c(HS-)=1×10-5mol/L | |
| B. | 稀释氨水溶液10倍后,其c(OH-)为原來的$\frac{1}{10}$ | |
| C. | pH之和为14的 H2C2O4与NaOH 溶液混合:c(Na+)+c(H+)=c(OH-)+C(HC2O4-) | |
| D. | 将等物质的费的Na2CO3和NaHCO3混合溶于水中:$\frac{c(C{O}_{{3}^{2-}})}{c(HC{O}_{{3}^{-}})}$<1 |