题目内容
1.锂空气电池是一种新型的二次电池,其放电时的工作原理如图所示,下列说法正确的是( )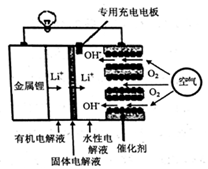
| A. | 正极区产生的LiOH可回收利用 | |
| B. | 电池中的有机电解液可以用稀盐酸代替 | |
| C. | 该电池放电时,正极的反应式为O2+4e-+4H+=2H2O | |
| D. | 该电池充电时,阴极发生了氧化反应:Li++e-=Li |
分析 在锂空气电池中,锂失电子作负极,负极是有机电解液,锂不与有该电解液直接反应,负极反应式为:4Li-4e-=4Li+,以空气中的氧气作为正极反应物,正极为水性电解液,氧气得电子生成氢氧根离子,正极反应为:O2+2H2O+4e-=4OH-,总反应为:4Li+O2+2H2O=4LiOH,据此解答.
解答 解:A.Li在负极失电子生成Li+,Li+向正极移动,正极区Li+与氢氧根离子结合形成LiOH,可以回收利用,故A正确;
B.金属锂能与盐酸反应生成氢气,所以电池中的有机电解液不可以用稀盐酸代替,故B错误;
C.正极上是氧气得电子生成氢氧根离子,则电极方程式为O2+4e-+2H2O=4OH-,故C错误;
D.阴极上阳离子得电子,则该电池充电时,阴极锂离子得电子发生还原反应:Li++e-═Li,故D错误;
故选A.
点评 本题考查了电化学基础知识,涉及电极判断、电极方程式书写、金属单质的性质等相关知识,侧重于基础知识的考查,题目难度不大.

练习册系列答案
相关题目
11.下列指定反应的离子方程式正确的是( )
| A. | FeCl3溶液中加少量氨水:Fe3++3OH-═Fe(OH)3↓ | |
| B. | 向Ba(OH)2溶液中加入过量的NH4HSO4溶液:Ba2++2OH-+NH${\;}_{4}^{+}$+H++SO${\;}_{4}^{2-}$═BaSO4↓+NH3•H2O+H2O | |
| C. | 惰性电极电解饱和NaCl溶液:2Cl-+2H+$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2 | |
| D. | 向Na2SO3溶液中滴加足量NaClO溶液:SO${\;}_{3}^{2-}$+ClO-═SO${\;}_{4}^{2-}$+Cl- |
12.下列溶液中的各组离子能大量共存的是( )
| A. | 含0.1 mol•L-1 CO32-的溶液中:Na+、K+、AlO2-、Cl- | |
| B. | 能与A1反应产生气泡的溶液中:Fe2+、Mg2+、I-、NO3-、 | |
| C. | 使酚酞变红的溶液中:NH4+、Al2+、Cl-、SO42- | |
| D. | 0.1 mol•L-1的盐酸中:Ca2+、K+、NO3-、HCO3- |
9.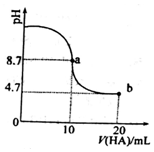 室温下向10mL0.1mol/L NaOH溶液中加入0.1mol/L的一元酸HA,溶液pH的变化曲线如闬所示.下列说法正确的是( )
室温下向10mL0.1mol/L NaOH溶液中加入0.1mol/L的一元酸HA,溶液pH的变化曲线如闬所示.下列说法正确的是( )
 室温下向10mL0.1mol/L NaOH溶液中加入0.1mol/L的一元酸HA,溶液pH的变化曲线如闬所示.下列说法正确的是( )
室温下向10mL0.1mol/L NaOH溶液中加入0.1mol/L的一元酸HA,溶液pH的变化曲线如闬所示.下列说法正确的是( )| A. | a 点所示溶液中 c(Na+)>c(A-)>c(H+)>c(HA) | |
| B. | a、b 两点所示溶液中水的电离程度相问 | |
| C. | b点所示溶液中c(A-)>c(HA) | |
| D. | pH=7时,c(Na+)-=c(A-)+c(HA) |
16.下列离子方程式错误的是( )
| A. | 向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| B. | (NH4) 2Fe (SO4) 2溶液与过量NaOH 溶液反应:Fe2++2OH-═Fe(OH)2↓ | |
| C. | 向 NaAlO2溶液中通过里 CO2:CO2+AlO2-+2H2O═Al(OH)3↓+HCO3- | |
| D. | 酸性 KMnO4 氧化 H2O2:MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O |
6.下列描述正确的是( )
| A. | 氨气溶于水能导电,所以氨气是电解质 | |
| B. | 硫粉在过量的纯氧中燃烧可以生成SO2 | |
| C. | 用过量氨水除去Fe3+溶液中的少量Al3+ | |
| D. | 所有铵盐受热均可以分解,产物均有NH3 |
13.下列说法正确的是( )
| A. | HNO3是挥发性一元酸 | |
| B. | Al2O3是金属氧化物、也是碱性氧化物 | |
| C. | 氧气和臭氧的相互转化是物理变化 | |
| D. | 利用过滤法可把Fe(OH)3胶体从FeCl3溶液中分离出来 |
4.仅用下列装置和表中所提供的物质(不考虑尾气处理,必要时可加热),能收集所制备的气体且能得出相应实验结论的是( )
| 选项 | ① | ② | ③ | 实验结论 | 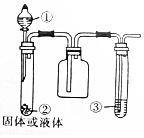 |
| A | 浓氨水 | 生石灰 | 石蕊试液 | 氨气是碱性气体 | |
| B | 浓硝酸 | 铜片 | 淀粉-KI溶液 | NO2水溶液具有氧化性 | |
| C | 浓硫酸 | 亚硫酸钠 | 酸性高锰酸钾溶液 | SO2具有漂白性 | |
| D | 浓盐酸 | 二氧化锰 | 紫色石蕊试液 | 氯气具有酸性和漂白性 |
| A. | A | B. | B | C. | C | D. | D |