9.在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是( )
| A. | 甲的摩尔体积比乙的摩尔体积小 | |
| B. | 甲的物质的量比乙的物质的量多 | |
| C. | 甲的相对分子质量比乙的相对分子质量小 | |
| D. | 甲的分子数比乙的分子数少 |
7.低温脱硝技术可用于处理废气中的氮氧化物发生的化学反应为:2NH3(g)+NO(g)+NO2(g)$?_{催化剂}^{180℃}$
2N2(g)+3H2O(g)△H<0 在恒容的密闭容器中,下列有关说法正确的是( )
2N2(g)+3H2O(g)△H<0 在恒容的密闭容器中,下列有关说法正确的是( )
| A. | 平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 | |
| B. | 平衡时,其他条件不变,增加 NH3 的浓度,废气中氮氧化物的转化率减小 | |
| C. | 其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 | |
| D. | 单位时间内消耗 NO 和 N2 的物质的量比为 1:2 时,反应达到平衡 |
6.在一定温度下将CO和水蒸气各1mol放在密闭容器中反应:CO+H2O?CO2+H2,达平衡后测得CO2为0.6mol.再通入4mol水蒸气,达到新的平衡后,CO2的物质的量为( )
| A. | 0.6 mol | B. | 1 mol | ||
| C. | >1 mol | D. | 0.6 mol<n(CO2)<1 mol |
5.已知2H2(g)+O2(g)→2H2O(g)+483.6kJ.下列说法或表达正确的是( )
| A. | 在相同的条件下,2mol 氢气与 1 mol 氧气的总能量小于2mol 水蒸气的总能量 | |
| B. | H2(g)+$\frac{1}{2}$O2(g)→H2O(1)+Q1;Q1>241.8kJ | |
| C. | H2(g)+$\frac{1}{2}$O2(g)→H2O(1)+Q2;Q2<241.8kJ | |
| D. | 任何条件下,2L水蒸气分解成2L氢气与1L氧气需吸收483.6kJ热量 |
4.下列说法正确的是( )
| A. | 在化学反应中,反应物转化为生成物的同时,必然发生能量的变化 | |
| B. | 放热反应中,反应物的总能量大于生成物的总能量 | |
| C. | 放热反应发生时不一定要加热,但吸热反应必须要加热才能发生 | |
| D. | 断开化学键的过程会放出能量 |
3.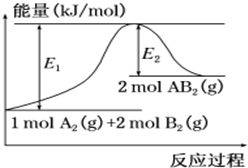 已知某化学反应A2 (g)+2B2 (g)═2AB2(g) (AB2的分子结构为B-A-B)的能量变化如图所示,下列有关叙述中正确的是( )
已知某化学反应A2 (g)+2B2 (g)═2AB2(g) (AB2的分子结构为B-A-B)的能量变化如图所示,下列有关叙述中正确的是( )
 已知某化学反应A2 (g)+2B2 (g)═2AB2(g) (AB2的分子结构为B-A-B)的能量变化如图所示,下列有关叙述中正确的是( )
已知某化学反应A2 (g)+2B2 (g)═2AB2(g) (AB2的分子结构为B-A-B)的能量变化如图所示,下列有关叙述中正确的是( )| A. | 该反应的进行一定需要加热 | |
| B. | 该反应的△H=-(E1-E2)kJ/mol | |
| C. | 该反应中反应物的键能总和大于生成物的键能总和 | |
| D. | 断裂1 mol A-A和2 mol B-B放出E1 kJ能量 |
2.Na2O2 和NO2都是中学化学常见的物质,某实验小组对他们之间的反应进行探究.
(1)小组同学对NO2 与Na2O2 的反应提出以下假设.
假设一:生成NaNO3,反应的化学方程式为2NO2+Na2O2═2NaNO3
假设二:生成NaNO2,反应的化学方程式为2NO2+Na2O2═2NaNO2+O2.
(2)小组同学在通风橱中制备并收集干燥的NO2 后进行如下实验:
①实验室常利用铜与浓硝酸反应制备NO2,反应的化学方程式为Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O.
②有同学根据实验1 中“气球变瘪”的现象推断假设一成立,你认为是否合理并简述理由:不能根据“气球变瘪”的现象推断假设一成立,理由是:根据方程式可以发现无论是按假设一还是假设二发生反应,体系的压强都要减小,都能观察到“气球变瘪”的现象.
(3)小组同学进一步对产物进行检验
查阅资料:
i.Na2O2 与水反应会生成H2O2;
ii.NO2-具有还原性,可用KMnO4 酸性溶液进行检验;
iii.含NO3-的溶液遇 FeSO4和浓硫酸生成棕色物质[Fe(NO)]2-
进行实验:
进行实验:
①实验2 的主要目的是排出溶液中H2O2对后续实验的干扰,请补全实验2 的操作向其中加入少量MnO2粉末,待不再产生气泡后,静置后取上层清液.
②根据实验3 的现象可得出结论“产物含”NO2-,该实验的现象是KMnO4溶液褪色.
③实验4 中进行步骤②的目的是通过和实验4步骤①进行对比,排除NO2-的存在对NO3-检验的干扰.
(4)该小组同学由以上全部实验可得出结论:Na2O2和NO2反应既能生成NaNO3也能生成NaNO2(或“假设一和假设二都成立”,或“Na2O2和NO2反应的产物中既含NO2-又含NO3-”).
0 159677 159685 159691 159695 159701 159703 159707 159713 159715 159721 159727 159731 159733 159737 159743 159745 159751 159755 159757 159761 159763 159767 159769 159771 159772 159773 159775 159776 159777 159779 159781 159785 159787 159791 159793 159797 159803 159805 159811 159815 159817 159821 159827 159833 159835 159841 159845 159847 159853 159857 159863 159871 203614
(1)小组同学对NO2 与Na2O2 的反应提出以下假设.
假设一:生成NaNO3,反应的化学方程式为2NO2+Na2O2═2NaNO3
假设二:生成NaNO2,反应的化学方程式为2NO2+Na2O2═2NaNO2+O2.
(2)小组同学在通风橱中制备并收集干燥的NO2 后进行如下实验:
| 序号 | 操作步骤 | 现象 |
| 实验1 | 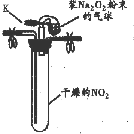 ①按如图组装仪器,打开K,将气球中的Na2O2粉末导入试管中,振荡,充分反应 | 试管内红棕色消失,气球变瘪 |
| ②试管冷却后,打开胶塞,加入5mL蒸馏水 | 未见红棕色气体,试管底部固体全部溶解得澄清溶液 |
②有同学根据实验1 中“气球变瘪”的现象推断假设一成立,你认为是否合理并简述理由:不能根据“气球变瘪”的现象推断假设一成立,理由是:根据方程式可以发现无论是按假设一还是假设二发生反应,体系的压强都要减小,都能观察到“气球变瘪”的现象.
(3)小组同学进一步对产物进行检验
查阅资料:
i.Na2O2 与水反应会生成H2O2;
ii.NO2-具有还原性,可用KMnO4 酸性溶液进行检验;
iii.含NO3-的溶液遇 FeSO4和浓硫酸生成棕色物质[Fe(NO)]2-
进行实验:
| 序号 | 操作步骤 | 现象 |
| 实验2 | 取实验1所得清液, 向其中加入少量MnO2粉末,待不再产生气泡后,静置后取上层清液,再调节此溶液pH至7左右 | / |
| 实验3 | 取实验2后的清液2mL,加入2滴0.1%的酸性KMnO4溶液 |
| 序号 | 操作步骤 | 现象 |
| 实验4 | ①向试管中加入2mL新制FeSO4溶液,再加入10滴0.1mol•L-1NaNO3溶液,振荡,再向试管中加入0.5mL98%的浓硫酸 | 滴入NaNO3溶液,无明显变化,加入浓硫酸后,溶液变棕色 |
| ②向试管中加入2mL新制FeSO4溶液,再加入10滴0.1mol•L-1NaNO2溶液,振荡,再向试管中加入0.5mL98%的浓硫酸 | 加入NaNO2溶液,立即变棕色,加入浓硫酸后,溶液无明显变化 | |
| ③向试管中加入2mL新制FeSO4溶液,再加入10滴实验2后的清液,振荡,再加0.5mL98%的浓硫酸 | 滴加实验2得到的清液后,溶液立即变浅棕色,加入浓硫酸后,溶液变深棕色 |
②根据实验3 的现象可得出结论“产物含”NO2-,该实验的现象是KMnO4溶液褪色.
③实验4 中进行步骤②的目的是通过和实验4步骤①进行对比,排除NO2-的存在对NO3-检验的干扰.
(4)该小组同学由以上全部实验可得出结论:Na2O2和NO2反应既能生成NaNO3也能生成NaNO2(或“假设一和假设二都成立”,或“Na2O2和NO2反应的产物中既含NO2-又含NO3-”).
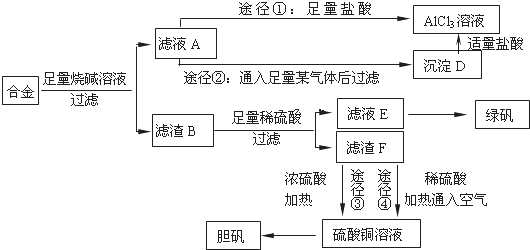
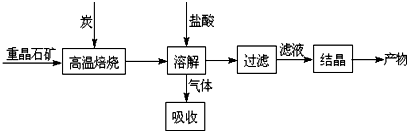
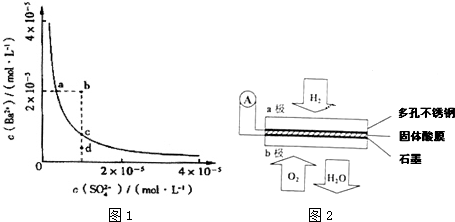
 分析图象回答:曲线②NO转化率随温度升高而增大的原因反应没有达到平衡,温度越高反应速率越快,转化率越大.在图2中画出反应2NO(g)+2CO(g)?N2(g)+2CO2(g)在不同温度下达到平衡时c(N2)的变化趋势图.
分析图象回答:曲线②NO转化率随温度升高而增大的原因反应没有达到平衡,温度越高反应速率越快,转化率越大.在图2中画出反应2NO(g)+2CO(g)?N2(g)+2CO2(g)在不同温度下达到平衡时c(N2)的变化趋势图.