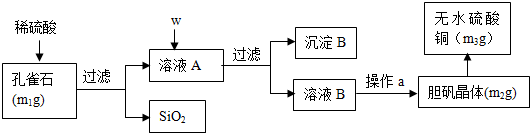
1.测定硫酸铜晶体(CuSO4•xH2O)结晶水含量的实验流程如下:
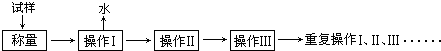
回答下列问题:
(1)以下是实验中可能用到的几种仪器,请在图下方横线上写出仪器名称.
a. 电子天平 b.
电子天平 b.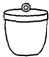 坩埚 c.
坩埚 c.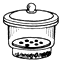 干燥器 d.
干燥器 d.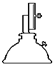 酒精喷灯
酒精喷灯
①“操作I”是灼烧硫酸铜晶体,用到上述bd(填序号)仪器.
②“操作Ⅱ”的操作是冷却,必须在c(填序号)中进行.
(2)“重复操作Ⅰ、Ⅱ、Ⅲ”,称为恒重操作.
判断达到恒重的依据是相邻两次称量的质量差小于0.001g;
进行恒重操作的目的是确保晶体失去全部结晶水.
(3)某学生实验后得到以表数据:
①根据以上数据计算该硫酸铜晶体中结晶水x的值为5.2(精确到0.1).
②该学生测定结果偏高(填“偏高”、“偏低”或“正确”).
③从下列分析中选出该学生产生实验误差的原因可能是(填序号)c.
a.没有进行恒重操作
b.加热固体到白色后,露置在空气中冷却
c.加热过程中晶体有少量溅失
d.加热后在干燥器中冷却至室温后称量.

回答下列问题:
(1)以下是实验中可能用到的几种仪器,请在图下方横线上写出仪器名称.
a.
 电子天平 b.
电子天平 b. 坩埚 c.
坩埚 c. 干燥器 d.
干燥器 d. 酒精喷灯
酒精喷灯①“操作I”是灼烧硫酸铜晶体,用到上述bd(填序号)仪器.
②“操作Ⅱ”的操作是冷却,必须在c(填序号)中进行.
(2)“重复操作Ⅰ、Ⅱ、Ⅲ”,称为恒重操作.
判断达到恒重的依据是相邻两次称量的质量差小于0.001g;
进行恒重操作的目的是确保晶体失去全部结晶水.
(3)某学生实验后得到以表数据:
| 加热前质量 | 加热后质量 | |
| m1(容器) | m2(容器+晶体) | m3(容器+无水硫酸铜) |
| 5.200g | 7.900g | 6.900g |
②该学生测定结果偏高(填“偏高”、“偏低”或“正确”).
③从下列分析中选出该学生产生实验误差的原因可能是(填序号)c.
a.没有进行恒重操作
b.加热固体到白色后,露置在空气中冷却
c.加热过程中晶体有少量溅失
d.加热后在干燥器中冷却至室温后称量.
19.某化学兴趣小组自行设计实验对废PET(聚对苯二甲酸乙二醇酯)进行化学解聚制备PET的初始原料对苯二甲酸(TPA)及乙二醇(EG),以实现治理污染、资源的循环利用.
查阅相关资料,得到主要试剂及产物的性质:
实验过程如下:
(一)解聚
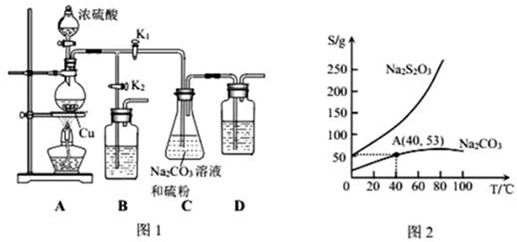
实验装置如图所示,A为三颈烧瓶,B为直形冷凝管,C为吸滤芯瓶,各接口均为玻璃接口.向装置中加入一定量废饮料瓶碎片及辅助试剂(催化剂、水等).缓慢搅拌,加热.待温度计上的温度显示高出200℃时,停止加热.则:
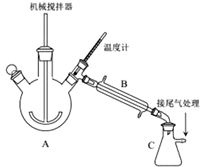
(1)写出聚对苯二甲酸乙二醇酯解聚的化学反应方程式: .
.
(2)C中收集到的是乙二醇;C装置吸滤瓶不能(填“能”或“不能”)换页成敞口锥形瓶,原因:乙二醇有毒,不能直接排放到空气中.
(3)成品聚对苯二甲酸乙二酯是一种结晶性好,无色透明,极为坚韧的材料.有玻璃的外观,无臭、无味、无毒,易燃,燃烧时,产生蓝色边缘的黄色火焰.其燃烧反应属于D.
A.聚合反应 B.加成聚合反应
C.综合聚合反应 D.高分子化学反应
(4)工业上生产“PET”的反应式为: ,生产时,若消耗EG的物质的量比TPA多4‰,则上述聚合物的链节数n为250.
,生产时,若消耗EG的物质的量比TPA多4‰,则上述聚合物的链节数n为250.
查阅相关资料,得到主要试剂及产物的性质:
| 物质 | 相对分子质量 | 性质 |
| 废饮料瓶碎片 | 聚对苯二甲酸乙二醇酯:乳白色或浅黄色的聚合物. | |
| 乙二醇(EG) | 62 | 无色无臭液体,对动物有毒性.沸点:196~198℃,与水混溶. |
对苯二甲酸(TPA) | 166 | 白色晶体或粉末,低毒.弱酸.300℃以上升华.不溶于水、乙醚、氯仿等大多数有机溶剂,可溶于DMF等强极性有机溶剂. |
(一)解聚
实验装置如图所示,A为三颈烧瓶,B为直形冷凝管,C为吸滤芯瓶,各接口均为玻璃接口.向装置中加入一定量废饮料瓶碎片及辅助试剂(催化剂、水等).缓慢搅拌,加热.待温度计上的温度显示高出200℃时,停止加热.则:

(1)写出聚对苯二甲酸乙二醇酯解聚的化学反应方程式:
 .
.(2)C中收集到的是乙二醇;C装置吸滤瓶不能(填“能”或“不能”)换页成敞口锥形瓶,原因:乙二醇有毒,不能直接排放到空气中.
(3)成品聚对苯二甲酸乙二酯是一种结晶性好,无色透明,极为坚韧的材料.有玻璃的外观,无臭、无味、无毒,易燃,燃烧时,产生蓝色边缘的黄色火焰.其燃烧反应属于D.
A.聚合反应 B.加成聚合反应
C.综合聚合反应 D.高分子化学反应
(4)工业上生产“PET”的反应式为:
 ,生产时,若消耗EG的物质的量比TPA多4‰,则上述聚合物的链节数n为250.
,生产时,若消耗EG的物质的量比TPA多4‰,则上述聚合物的链节数n为250.
17.乙酸正丁酯是无色透明有愉快果香气味的液体,可由乙酸和正丁醇制备.反应的化学方程式如下:
CH3COOH+CH2CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O
发生的副反应如下:2CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$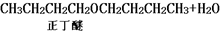
CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$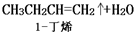
有关化合物的物理性质见表:
已知:乙酸正丁酯、正丁醇和水组成三元共沸物恒沸点为90.7℃.
合成:
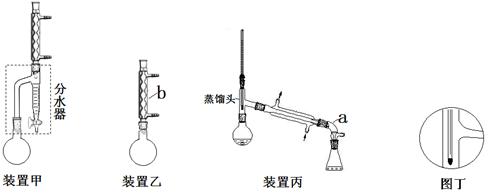
方案甲:采用装置甲(分水器预先加入水,使水面略低于分水器的支管口),在干燥的50mL圆底烧瓶中,加入13.8mL(0.150mol)正丁醇和7.2mL(0.125mol)冰醋酸,再加入3~4滴浓硫酸和2g沸石,摇匀.按下图安装好带分水器的回流反应装置,通冷却水,圆底烧瓶在电热套上加热煮沸.在反应过程中,通过分水器下部的旋塞分出生成的水(注意保持分水器中水层液面仍保持原来高度,使油层尽量回到圆底烧瓶中).反应基本完成后,停止加热.
方案乙:采用装置乙,加料方式与方案甲相同.加热回流,反应60min后停止加热.
提纯:甲乙两方案均采用蒸馏方法.操作如下:

请回答:
(1)方案甲中使用分水器不断分离除去水的目的是有利于平衡向生成乙酸正丁酯的反应方向移动.
(2)仪器a的名称接受器或牛角管,仪器b的名称球形冷凝管.
(3)提纯过程中,步骤②的目的是为了除去有机层中残留的酸,步骤④加入少量无水MgSO4的目的是干燥.
(4)下列有关洗涤过程中分液漏斗的使用正确的是AB.
A.分液漏斗使用前必须要检漏,只要分液漏斗的玻璃塞和旋塞芯处不漏水即可使用
B.洗涤时振摇放气操作应如图所示

C.放出下层液体时,不需将要玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔
D.洗涤完成后,先放出下层液体,然后继续从下口放出有机层置于干燥的锥形瓶中
(5)按装置丙蒸馏,最后圆底烧瓶中残留的液体主要是正丁醚;若按图丁放置温度计,则收集到的产品馏分中还含有正丁醇.
(6)实验结果表明方案甲的产率较高,原因是通过分水器及时分离出产物水,有利于酯化反应的进行,提高酯的产率.
CH3COOH+CH2CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O
发生的副反应如下:2CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$
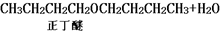
CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$
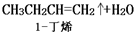
有关化合物的物理性质见表:
| 化合物 | 密度(g•cm-3) | 水溶性 | 沸点(℃) |
| 冰乙酸 | 1.05 | 易溶 | 118.1 |
| 正丁醇 | 0.80 | 微溶 | 117.2 |
| 正丁醚 | 0.77 | 不溶 | 142.0 |
| 乙酸正丁酯 | 0.90 | 微溶 | 126.5 |
合成:
方案甲:采用装置甲(分水器预先加入水,使水面略低于分水器的支管口),在干燥的50mL圆底烧瓶中,加入13.8mL(0.150mol)正丁醇和7.2mL(0.125mol)冰醋酸,再加入3~4滴浓硫酸和2g沸石,摇匀.按下图安装好带分水器的回流反应装置,通冷却水,圆底烧瓶在电热套上加热煮沸.在反应过程中,通过分水器下部的旋塞分出生成的水(注意保持分水器中水层液面仍保持原来高度,使油层尽量回到圆底烧瓶中).反应基本完成后,停止加热.
方案乙:采用装置乙,加料方式与方案甲相同.加热回流,反应60min后停止加热.

提纯:甲乙两方案均采用蒸馏方法.操作如下:

请回答:
(1)方案甲中使用分水器不断分离除去水的目的是有利于平衡向生成乙酸正丁酯的反应方向移动.
(2)仪器a的名称接受器或牛角管,仪器b的名称球形冷凝管.
(3)提纯过程中,步骤②的目的是为了除去有机层中残留的酸,步骤④加入少量无水MgSO4的目的是干燥.
(4)下列有关洗涤过程中分液漏斗的使用正确的是AB.
A.分液漏斗使用前必须要检漏,只要分液漏斗的玻璃塞和旋塞芯处不漏水即可使用
B.洗涤时振摇放气操作应如图所示

C.放出下层液体时,不需将要玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔
D.洗涤完成后,先放出下层液体,然后继续从下口放出有机层置于干燥的锥形瓶中
(5)按装置丙蒸馏,最后圆底烧瓶中残留的液体主要是正丁醚;若按图丁放置温度计,则收集到的产品馏分中还含有正丁醇.
(6)实验结果表明方案甲的产率较高,原因是通过分水器及时分离出产物水,有利于酯化反应的进行,提高酯的产率.
14.可逆反应2HI(气)?H2(气)+I2(气)达到平衡后,当改变外界条件(如某一物质浓度、体系压强、温度等)而发生下列项目的变化时,能作为平衡一定发生了移动的标志是( )
0 159639 159647 159653 159657 159663 159665 159669 159675 159677 159683 159689 159693 159695 159699 159705 159707 159713 159717 159719 159723 159725 159729 159731 159733 159734 159735 159737 159738 159739 159741 159743 159747 159749 159753 159755 159759 159765 159767 159773 159777 159779 159783 159789 159795 159797 159803 159807 159809 159815 159819 159825 159833 203614
| A. | 气体的密度发生了变化 | B. | 气体的平均分子量发生了变化 | ||
| C. | 气体的颜色发生了变化 | D. | 体系的温度发生了变化 |