11.图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为 .
.
(2)地壳中含量最多的金属元素是Al.写出元素⑥的最简单氢化物的化学式CH4.
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
(4)写出③、④、⑤对应离子氧化性由强到弱的是Al3+>Mg2+>Na+,②、⑦、⑩对应氢化物酸性由强到弱的是HBr>HCl>HF.
(5)写出⑤与氢氧化钠溶液反应的化学方程式:2Al+2NaOH+2H2O═2NaAlO2+3H2↑..
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ⑥ | ① | ② | |||||
| 三 | ③ | ④ | ⑤ | ⑪ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
 .
.(2)地壳中含量最多的金属元素是Al.写出元素⑥的最简单氢化物的化学式CH4.
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
(4)写出③、④、⑤对应离子氧化性由强到弱的是Al3+>Mg2+>Na+,②、⑦、⑩对应氢化物酸性由强到弱的是HBr>HCl>HF.
(5)写出⑤与氢氧化钠溶液反应的化学方程式:2Al+2NaOH+2H2O═2NaAlO2+3H2↑..
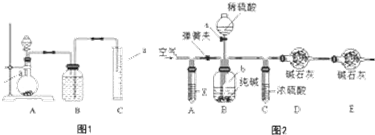
9.硫酸具有重要的用途,某工厂用如图2示的工艺流程生产硫酸.

请回答下列问题:
(1)与以硫铁矿为原料的生产工艺相比,该工艺的特点是A.
A.耗氧量减少 B.二氧化硫的转化率提高
C.产生的废渣减少 D.不需要使用催化剂
(2)气体a的成分是二氧化硫和氧气.
(3)进入接触室的气体,须先经过净化室的原因是防止混合气体中的灰尘、水蒸气等在接触室中导致催化剂中毒.
①吸收塔中吸收SO3的物质名称是98.3%浓硫酸.
②以SO2和O2为原料,利用电化学原理也可以制备硫酸,装置如图2电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触.B极的电极反应式为SO2-2e-+2H2O═SO42-+4H+.
③吸收塔排出的尾气先用氨水吸收,得到铵盐M,再用浓硫酸 处理M,得到较髙浓度的SO2.SO2既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的Br2.SO2吸收Br2时发生反应的离子方程式是SO2-2e-+2H2O═SO42-+4H+.
④为确定③中铵盐M的成分,将不同质量的铵盐分别加入50.00ml相同浓度的NaOH溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解),测得标准状况下NH3的体积如表:
该铵盐的成分是NH4HSO3和(NH4)2SO3,其物质的量之比是1:1.

请回答下列问题:
(1)与以硫铁矿为原料的生产工艺相比,该工艺的特点是A.
A.耗氧量减少 B.二氧化硫的转化率提高
C.产生的废渣减少 D.不需要使用催化剂
(2)气体a的成分是二氧化硫和氧气.
(3)进入接触室的气体,须先经过净化室的原因是防止混合气体中的灰尘、水蒸气等在接触室中导致催化剂中毒.
①吸收塔中吸收SO3的物质名称是98.3%浓硫酸.
②以SO2和O2为原料,利用电化学原理也可以制备硫酸,装置如图2电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触.B极的电极反应式为SO2-2e-+2H2O═SO42-+4H+.
③吸收塔排出的尾气先用氨水吸收,得到铵盐M,再用浓硫酸 处理M,得到较髙浓度的SO2.SO2既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的Br2.SO2吸收Br2时发生反应的离子方程式是SO2-2e-+2H2O═SO42-+4H+.
④为确定③中铵盐M的成分,将不同质量的铵盐分别加入50.00ml相同浓度的NaOH溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解),测得标准状况下NH3的体积如表:
| 铵盐的质量/g | 2.15 | 4.30 | 6.45 |
| NH3的体积/mL | 672 | 1344 | 1344 |
8.从浓度为98%,密度为1.84g•cm-3的浓硫酸试剂瓶中取出10mL的浓硫酸,然后稀释至1L,则所得稀硫酸的物质的量浓度为( )
| A. | 1.84 mol•L-1 | B. | 18.4 mol•L-1 | C. | 0.184 mol•L-1 | D. | 0.018 4 mol•L-1 |
3.某酸性FeSO3溶液中含有少量的SnSO4,为得到纯净的硫酸亚铁晶体(FeSO4•xH2O),可向溶液中通入H2S气体至饱和,然后用硫酸酸化至pH=2,过滤后,将所得滤液蒸发浓缩、冷却结晶、过滤洗涤,得到硫酸亚铁晶体.查阅资料,得到相关物质的有关数据如表:
(1)用硫酸亚铁晶体配置FeSO4溶液时还需加入的物质是铁粉和稀硫酸;
(2)为检验制得的硫酸亚铁晶体中是否含有Fe3+,可选用的试剂为AC;
A.KSCN溶液B.稀硫酸C.淀粉-KI溶液D.KMnO4溶液
(3)通入H2S气体至饱和的目的是除去溶液中的Sn2+离子,并防止Fe2+被氧化;用硫酸酸化至pH=2的目的是防止Fe2+离子生成沉淀;
(4)为研究硫酸亚铁晶体的热分解,某兴趣小组同学称取ag硫酸亚铁晶体样品,按图1装置进行高温加热,使其完全分解(硫酸亚铁晶体在高温条件下回分解为三种化合物和一种单质,该单质能使带火星的木条复燃),对所得产物进行探究,并通过称量装置B的质量测出x的值.
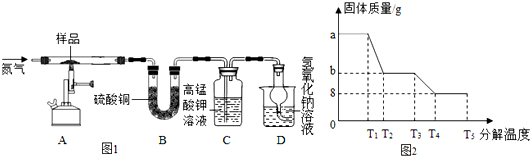
①装置B中午睡硫酸铜粉末变蓝,质量增加12.6g,说明产物中有水,装置C中高锰酸钾溶液褪色,说明产物中含有二氧化硫;
②实验中要持续通入氮气,否则测出的x会偏小(填“偏大”、“偏小”或“不变”);
③硫酸亚铁晶体完全分解后装置A中固体呈红棕色,将其加入足量稀盐酸中,固体全部溶解,得黄色溶液;
④某研究所利用SDTQ600热分析仪对硫酸亚铁晶体进行热分解,获得相关数据,绘制成的固体质量与分解温度的关系图如图2,根据图中有关数据,可计算出x为7.
| 25℃ | pH | 25℃ | pH |
| 饱和H2S溶液 | 3.9 | FeS开始沉淀 | 3.0 |
| SnS沉淀完全 | 1.6 | FeS沉淀完全 | 5.5 |
(2)为检验制得的硫酸亚铁晶体中是否含有Fe3+,可选用的试剂为AC;
A.KSCN溶液B.稀硫酸C.淀粉-KI溶液D.KMnO4溶液
(3)通入H2S气体至饱和的目的是除去溶液中的Sn2+离子,并防止Fe2+被氧化;用硫酸酸化至pH=2的目的是防止Fe2+离子生成沉淀;
(4)为研究硫酸亚铁晶体的热分解,某兴趣小组同学称取ag硫酸亚铁晶体样品,按图1装置进行高温加热,使其完全分解(硫酸亚铁晶体在高温条件下回分解为三种化合物和一种单质,该单质能使带火星的木条复燃),对所得产物进行探究,并通过称量装置B的质量测出x的值.

①装置B中午睡硫酸铜粉末变蓝,质量增加12.6g,说明产物中有水,装置C中高锰酸钾溶液褪色,说明产物中含有二氧化硫;
②实验中要持续通入氮气,否则测出的x会偏小(填“偏大”、“偏小”或“不变”);
③硫酸亚铁晶体完全分解后装置A中固体呈红棕色,将其加入足量稀盐酸中,固体全部溶解,得黄色溶液;
④某研究所利用SDTQ600热分析仪对硫酸亚铁晶体进行热分解,获得相关数据,绘制成的固体质量与分解温度的关系图如图2,根据图中有关数据,可计算出x为7.
2.X、Y、Z、R、W是5种短周期元素,原子序数依次增大;它们可组成离子化合物Z2Y和共价化合物RY3、XW4;已知Y、R同主族,Z、R、W同周期.下列说法错误的是( )
0 159472 159480 159486 159490 159496 159498 159502 159508 159510 159516 159522 159526 159528 159532 159538 159540 159546 159550 159552 159556 159558 159562 159564 159566 159567 159568 159570 159571 159572 159574 159576 159580 159582 159586 159588 159592 159598 159600 159606 159610 159612 159616 159622 159628 159630 159636 159640 159642 159648 159652 159658 159666 203614
| A. | 原子半径:Z>R>W | |
| B. | 气态氢化物稳定性:HmW>HnR | |
| C. | XW4分子中各原子均满足8电子结构 | |
| D. | Y、Z、R三种元素组成的化合物水溶液一定显碱性 |

 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ +CO2↑
+CO2↑ $→_{△}^{NaOH(aq)}$
$→_{△}^{NaOH(aq)}$ +H2O
+H2O $→_{(Ⅱ)H+}^{(Ⅰ)_{10}%NaOH;Cu}$
$→_{(Ⅱ)H+}^{(Ⅰ)_{10}%NaOH;Cu}$
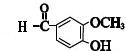 +CH3COCH2COCH3$→_{△}^{NaOH(aq)}$
+CH3COCH2COCH3$→_{△}^{NaOH(aq)}$ +2H2O.
+2H2O.

 ,其中含有的化学键类型为离子键和共价键.
,其中含有的化学键类型为离子键和共价键.