题目内容
11.图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ⑥ | ① | ② | |||||
| 三 | ③ | ④ | ⑤ | ⑪ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
 .
.(2)地壳中含量最多的金属元素是Al.写出元素⑥的最简单氢化物的化学式CH4.
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
(4)写出③、④、⑤对应离子氧化性由强到弱的是Al3+>Mg2+>Na+,②、⑦、⑩对应氢化物酸性由强到弱的是HBr>HCl>HF.
(5)写出⑤与氢氧化钠溶液反应的化学方程式:2Al+2NaOH+2H2O═2NaAlO2+3H2↑..
分析 由元素在周期表中的位置可知,①为N、②为F、③为Na、④为Mg、⑤为Al、⑥为C、⑦为Cl、⑧为Ar、⑨为K、⑩为Br、⑪为Si,
(1)稀有气体Ar最不活泼,原子核外有18个电子,有3个电子层,各层电子数为2、8、8;
(2)地壳中含量较多的元素依次是氧、硅、铝、铁,其中铝、铁是金属元素;元素⑥为碳,CH4是最简单的有机化合物;
(3)元素周期表右上方的非金属性最强,0族元素除外,但元素最高价氧化物的水化物中高氯酸是最强酸,最强的含量K的金属性最强,其最高价氧化物对应水化物的碱性最强;氢氧化铝是两性氢氧化物;
(4)③、④、⑤均为金属元素,金属越活泼,对应阳离子的氧化性越弱,Al是其中金属性最弱的金属元素;②、⑦、⑩对就的氢化物依次为HF、HCl、HBr,其水溶液的酸性依次增强,其中HF为弱酸,其余均为强酸;
(5)Al与氢氧化钠溶液反应生成偏铝酸钠与氢气.
解答 解:由元素在周期表中的位置可知,①为N、②为F、③为Na、④为Mg、⑤为Al、⑥为C、⑦为Cl、⑧为Ar、⑨为K、⑩为Br、⑪为Si;
(1)稀有气体Ar最不活泼,原子核外有18个电子,有3个电子层,各层电子数为2、8、8,原子结构示意图为: ,
,
故答案为: ;
;
(2)Al是地壳中含量最高的金属元素,碳的最简单氢化物为CH4,故答案为:Al;CH4;
(3)氯元素最高价氢化物对应水化物HClO4是最强酸,K的金属性最强,KOH碱性最强;氢氧化铝是两性氢氧化物,故答案为:HClO4;KOH;Al(OH)3;
(4)Na、Mg、Al三种金属元素对应阳离子氧化性由强到弱的顺序为Al3+>Mg2+>Na+;F、Cl、Br三种元素的氢化物水溶液酸性由强到弱的顺序为HBr>HCl>HF;故答案为:Al3+>Mg2+>Na+;HBr>HCl>HF;
(6)铝与氢氧化钠溶液反应生成偏铝酸钠与氢气,反应方程式为2Al+2NaOH+2H2O═2NaAlO2+3H2↑,
故答案为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
点评 本题考查元素周期表与元素周期律综合应用,难度不大,注意整体把握元素周期表结构,熟练掌握基础知识.

(1)PbO2具有强氧化性,在加热时可与浓盐酸反应制Cl2,发生的化学方程式为PbO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$PbCl2+Cl2↑+2H2O;
(2)Fe3O4属于混合氧化物,其组成可表示为FeO•Fe2O3,Pb3O4和Fe3O4一样,也属于混合氧化物,其组成也可表示为2PbO•PbO2;
PbO也是一种重要的物质.工业上生产锌钡白(ZnS•BaSO4)的过程中,会产生含CaSO4、PbSO4的废渣,实验室利用该废渣生产PbO的流程如下.
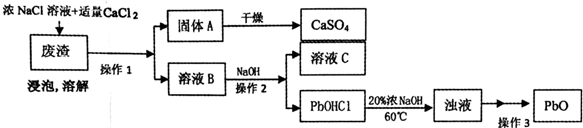
过程中发生的部分反应如下:
浸泡:PbSO4(s)+2Cl-(aq)═PbCl2(s)+SO42-(aq)
溶解:PbC12+2Cl-=PbCl42-;PbCl42-+OH-=PbOHCl↓+3Cl-
有关数据:不同温度和浓度的食盐溶液中PbC12的溶解度(g/L)
NaCl浓度(g/L)温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | 180 | 260 | 300 |
| 13 | 7 | 3 | 1 | 0 | 0 | 0 | 3 | 9 | 13 |
| 50 | 11 | 8 | 4 | 3 | 4 | 5 | 10 | 21 | 35 |
| 100 | 21 | 17 | 11 | 12 | 13 | 15 | 30 | 65 | 95 |
(4)溶液C中的溶质主要成份是NaCl,在实验室里,将溶质分离出来需要用到的玻璃仪器有酒精灯、玻璃棒;
(5)实验时,取用废渣50.0g,实验过程中PbSO4的转化率为100%,CaSO4的损耗率为5%,最后得到干燥的CaSO4固体39.6g,则废渣中PbSO4的质量分数为30.2%(用百分数表示,精确到小数点后一位).
| A. | 反应生成了1.12L(标准状况)H2 | |
| B. | 向反应后的溶液中加入足量小苏打,最终有白色沉淀生成 | |
| C. | 在反应后的溶液中一定能大量共存的粒子有:K+、Mg2+、I-、NO3- | |
| D. | 向反应后的溶液中加入足量稀硫酸,最终有白色沉淀生成 |
| A. | $\frac{3n+2}{2}$ | B. | $\frac{3n-2}{2}$ | C. | $\frac{2n-2}{3}$ | D. | n+1 |
| A. | Na2CO3和H2SO4 | B. | AlC13和NaOH | C. | NaAlO2和H2SO4 | D. | NaHCO3和Ba(OH)2 |

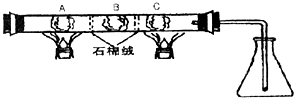 在一硬质玻璃管中进行如图所示的实验,图中A为NH4HCO3,B为Na2O2,C为Pt丝;石棉绒起隔离药品的作用.充分反应后,发现锥形瓶内出现红棕色气体,随之又有白烟产生.
在一硬质玻璃管中进行如图所示的实验,图中A为NH4HCO3,B为Na2O2,C为Pt丝;石棉绒起隔离药品的作用.充分反应后,发现锥形瓶内出现红棕色气体,随之又有白烟产生.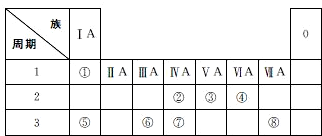
 .
.