10.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 25℃时,pH=7的NH4Cl和NH3•H2O的混合溶液中,OH-数为10-7NA | |
| B. | 33.6 L NO2溶于足量的水得到的溶液中含有的NO3-数为NA | |
| C. | P4O6的分子结构中只含有单键,且每个原子的最外层都满足8电子结构,则1 mol该分子中含有的共价键数目是10NA | |
| D. | 18g的D2O与NA个-CH3具有相同的电子数 |
9.下列有关化学与生活、工业的叙述中,正确的是( )
| A. | 去年12月我国向月球发射的“玉兔号”月亮车,体现了我国航天科技的实力,车上安装的太阳能电池帆板的材料是二氧化硅 | |
| B. | 水泥冶金厂常用高压电除去工厂烟尘,利用了胶体的性质 | |
| C. | 中国食品质量监督局规定,从2011年5月份起,面粉中禁止添加CaO2、过氧化苯甲酰等增白剂,由此说明添加剂均会严重危害人体健康 | |
| D. | 以煤为燃料的工厂、汽车尾气排放物等容易造成雾霾,治理雾霾最好的办法是研制纳米级口罩,以确保肺癌的发病率降低 |
8.如图1所示是实验室中制取气体的一种简易装置.
(1)请简述检验它的气密性的方法关闭止水夹,从左管处加水,使U形管两端形成液面差,一段时间后,液面差没有变化,说明气密性良好.
(2)利用如图1所示装置可以制取(填反应物状况及发生反应是否需要的条件)不溶于水的块状固体、不需要加热而反应生成的气体.
某同学设计如图2所示装置,用粗铁粒与16.9%稀硝酸反应制取NO气体并探究产物中铁的价态.请回答有关问题.

(3)已知16.9%稀硝酸的密度为1.10g/cm3,则其物质的量浓度为2.95mol/L(计算结果保留两位小数).用若用63%的硝酸配制16.9%稀硝酸500mL,所需的玻璃仪器有玻璃棒、烧杯和量筒.
(4)当打开止水夹a、关闭止水夹b时,A装置的干燥管中观察到的现象是有红棕色气体出现.B装置烧杯中液体的作用是吸收NO2.当A装置中气体几乎无色时,打开止水夹b,关闭止水夹a,可用C装置收集NO气体.
(5)已知下列反应可以发生:Fe2O3+3KNO3+4KOH$\stackrel{高温}{→}$2K2FeO4+3KNO2+2H2O,而A装置中的稀硝酸即使换成浓硝酸,也不能生成+6价的铁的化合物,其原因是d.
a.HNO3的氧化性比KNO3弱 b.反应的温度不够
c.HNO3的热稳定性比KNO3差 d.FeO42-不能存在于酸性溶液中
(6)现有仪器和药品:试管和胶头滴管,0.1mol/LKSCN溶液、0.2mol/L酸性KMnO4溶液、0.1mol/LKI溶液、氯水等.请设计一个简单实验,探究A装置烧杯里完全反应后含铁可能的价态,填写下列实验报告:
(1)请简述检验它的气密性的方法关闭止水夹,从左管处加水,使U形管两端形成液面差,一段时间后,液面差没有变化,说明气密性良好.
(2)利用如图1所示装置可以制取(填反应物状况及发生反应是否需要的条件)不溶于水的块状固体、不需要加热而反应生成的气体.
某同学设计如图2所示装置,用粗铁粒与16.9%稀硝酸反应制取NO气体并探究产物中铁的价态.请回答有关问题.

(3)已知16.9%稀硝酸的密度为1.10g/cm3,则其物质的量浓度为2.95mol/L(计算结果保留两位小数).用若用63%的硝酸配制16.9%稀硝酸500mL,所需的玻璃仪器有玻璃棒、烧杯和量筒.
(4)当打开止水夹a、关闭止水夹b时,A装置的干燥管中观察到的现象是有红棕色气体出现.B装置烧杯中液体的作用是吸收NO2.当A装置中气体几乎无色时,打开止水夹b,关闭止水夹a,可用C装置收集NO气体.
(5)已知下列反应可以发生:Fe2O3+3KNO3+4KOH$\stackrel{高温}{→}$2K2FeO4+3KNO2+2H2O,而A装置中的稀硝酸即使换成浓硝酸,也不能生成+6价的铁的化合物,其原因是d.
a.HNO3的氧化性比KNO3弱 b.反应的温度不够
c.HNO3的热稳定性比KNO3差 d.FeO42-不能存在于酸性溶液中
(6)现有仪器和药品:试管和胶头滴管,0.1mol/LKSCN溶液、0.2mol/L酸性KMnO4溶液、0.1mol/LKI溶液、氯水等.请设计一个简单实验,探究A装置烧杯里完全反应后含铁可能的价态,填写下列实验报告:
| 实验步骤 | 操作 | 现象与结论 |
| 第一步 | 取少量液体装于试管,向试管中滴入几滴KSCN溶液. | |
| 第二步 | 若溶液紫色褪去,则说明含有Fe2+; 若无明显变化,则说明不含Fe2+. |
6.电浮选凝聚法是工业上采用的一种污水处理方法,某研究小组用电浮选凝聚法处理污水,设计装置如图所示,下列说法不正确的是( )
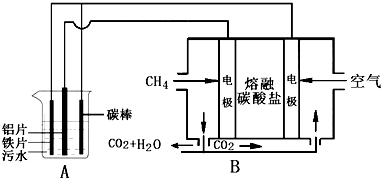

| A. | 装置B中通CH4一极电极反应为:CH4+4CO32--8e-═5CO2+2H2O | |
| B. | 装置B中CO32-向CH4一极移动 | |
| C. | A中阳极相关反应有:Fe-2e-═Fe2+ 2H2O-4e-═4H++O2↑ 12Fe2++3O2+6H2O═4Fe(OH)3↓+8Fe3+ | |
| D. | 标准状况下,若A装置中产生44.8 L气体,则理论上B装置中要消耗CH411.2L |
5.下列离子方程式正确的是( )
| A. | 高锰酸钾溶液与乙二酸(草酸)反应:2MnO4-+5C2O42-+16H+→2Mn2++10CO2↑+8H2O | |
| B. | 苯酚与碳酸钠溶液: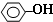 +CO32-→ +CO32-→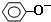 +H2CO3 +H2CO3 | |
| C. | 等体积等物质的量浓度的NH4Fe(SO4)2和Ba(OH)2混合:2Fe3++3SO42-+3Ba2++6OH-═3BaSO4↓+2Fe(OH)3↓ | |
| D. | 在强碱性溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3═2FeO42-+3Cl-+H2O+4H+ |
4.下列说法正确的是( )
| A. | 前四周期中最外层电子数大于或等于3的元素一定是主族元素 | |
| B. | 冰中水分子空隙大于4℃液态水、近沸点水蒸汽中存在(H2O)n与形成配位键有关 | |
| C. | 化合物中某元素为+1价,则表明失去了1个电子且带1个单位正电荷 | |
| D. | 在化学反应中,原子首先失去的电子能量最低 |
3.常温下,下列溶液中微粒的物质的量浓度关系正确的是( )
| A. | 0.1 mol/LCH3COONa溶液与0.1 mol/LCaCl2溶液等体积混合:c(Na+)+c(Ca2+)═c(CH3COO-)+c(CH3COOH)+2c(Cl- ) | |
| B. | 将等体积、等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体后的溶液:c(H+)+c(H2CO3)═c(OH-)+c(CO32-)+c(NH3•H2O) | |
| C. | 0.1 mol/LCH3COONa溶液与0.1 mol/LHCl溶液混合至pH=7:c(Na+)>c(Cl-)=c(CH3COOH)>c(CH3COO-) | |
| D. | 0.2mol/L氨水与0.1 mol/LHCl溶液等体积混合:c(Cl-)+c(H+)═c(NH3•H2O)+c(OH-) |
2.下列化学反应的离子方程式正确的是( )
| A. | Ba(OH)2溶液中滴加NH4HSO4溶液至Ba2+沉淀完全:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| B. | 将过量SO2气体通入氨水中:SO2+NH3•H2O═NH4++HSO3- | |
| C. | 用醋酸除去水垢中的CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | 用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O═3I2+6OH- |
1.短周期主族元素X、Y、Z、W的原子序数依次增大.其中X、Z同主族,Z的单质是一种良好的半导体材料,Y元素原子最外层电子数等于其电子层数,W是同周期中原子半径最小的元素.下列叙述正确的是( )
0 156629 156637 156643 156647 156653 156655 156659 156665 156667 156673 156679 156683 156685 156689 156695 156697 156703 156707 156709 156713 156715 156719 156721 156723 156724 156725 156727 156728 156729 156731 156733 156737 156739 156743 156745 156749 156755 156757 156763 156767 156769 156773 156779 156785 156787 156793 156797 156799 156805 156809 156815 156823 203614
| A. | Y的简单离子半径小于W的简单离子半径 | |
| B. | W、X形成的化合物为离子化合物 | |
| C. | X的最高价氧化物对应的水化物的酸性比W的强 | |
| D. | Z的气态简单氢化物的稳定性比X的强 |
 .
.