题目内容
6.电浮选凝聚法是工业上采用的一种污水处理方法,某研究小组用电浮选凝聚法处理污水,设计装置如图所示,下列说法不正确的是( )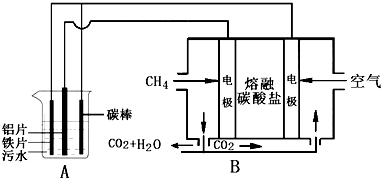
| A. | 装置B中通CH4一极电极反应为:CH4+4CO32--8e-═5CO2+2H2O | |
| B. | 装置B中CO32-向CH4一极移动 | |
| C. | A中阳极相关反应有:Fe-2e-═Fe2+ 2H2O-4e-═4H++O2↑ 12Fe2++3O2+6H2O═4Fe(OH)3↓+8Fe3+ | |
| D. | 标准状况下,若A装置中产生44.8 L气体,则理论上B装置中要消耗CH411.2L |
分析 燃料电池中,正极发生的反应是氧气得电子被还原的过程,负极发生的反应是燃料失电子被氧化的过程;电池是以熔融碳酸盐为电解质,可以循环利用的物质只有二氧化碳,甲烷燃料电池中,负极发生的反应是甲烷失电子被氧化的过程,电极反应式为CH4+4CO32--8e-=5CO2+2H2O,所以电解时铁作阳极,因此主要发生Fe-2e-=Fe2+,阴极上氢离子得电子生成氢气,以此解答该题.
解答 解:A.甲烷燃料电池中,负极发生的反应是甲烷失电子被氧化的过程,电极反应式为:CH4+4CO32--8e-=5CO2+2H2O,故A正确;
B.原电池工作时,阴离子向负极移动,故B正确;
C.铁为阳极,可被氧化生成亚铁离子,碳棒上可生成氧气,氧气和亚铁离子生成氢氧化铁,可用于净水,故C正确;
D.A装置中阴极的电极反应为:2H++2e-=H2↑,阴极产生了44.8L(标准状况)即2mol的气体产生,但是碳棒为阳极,阳极上还可以生成氧气,所以参加反应的甲烷大于11.2L,故D错误.
故选D.
点评 本题考查原电池和电解池工作原理,较为综合,题目难度中等,做题时注意利用守恒的思考去解答,同时注意电极反应式的书写方法,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
17.欲配制浓度为1.00mol/L的氯化钠溶液100mL,用不到的仪器是( )
| A. | 100mL容量瓶 | B. | 分液漏斗 | C. | 玻璃棒 | D. | 胶头滴管 |
1.短周期主族元素X、Y、Z、W的原子序数依次增大.其中X、Z同主族,Z的单质是一种良好的半导体材料,Y元素原子最外层电子数等于其电子层数,W是同周期中原子半径最小的元素.下列叙述正确的是( )
| A. | Y的简单离子半径小于W的简单离子半径 | |
| B. | W、X形成的化合物为离子化合物 | |
| C. | X的最高价氧化物对应的水化物的酸性比W的强 | |
| D. | Z的气态简单氢化物的稳定性比X的强 |
18.NA表示阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 用铜作电极电解饱和食盐水,当线路中通过NA个电子时,阳极生成11.2L气体(标准状况下) | |
| B. | 把5.6g铁片投入到足量的冷的浓硝酸中,转移电子数为0.3NA | |
| C. | 12g石墨晶体中含有碳碳单键数为1.5NA | |
| D. | 15g-CH3中含有的电子数为10NA |
15.低血糖患者常需补充葡萄糖.组成葡萄糖的元素有( )
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
16.NA为阿伏加德罗常数,下列说法不正确的是( )
| A. | 4.0gCuO和Cu2S的混合物含铜离子个数为0.05NA | |
| B. | 标准状况下,11.2LC5H12蒸气所含甲基数目最多为NA | |
| C. | 0.5molK与O2完全反应生成K2O,K2O2,KO3的混合物,转移电子数为0.5NA | |
| D. | 1L 0.2mol•L-1HI溶液中含I-数目为0.2NA |

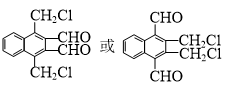 .
.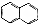 )的衍生物,且取代基都在同一个苯环上;
)的衍生物,且取代基都在同一个苯环上;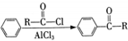 (R为烃基).根据已有知识并结合相关信息,写出以ClCH2CH2CH2Cl和
(R为烃基).根据已有知识并结合相关信息,写出以ClCH2CH2CH2Cl和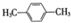 为原料制备
为原料制备 的合成路线流程图(无机试剂可任选).合成路线流程图示例如图所示:
的合成路线流程图(无机试剂可任选).合成路线流程图示例如图所示: