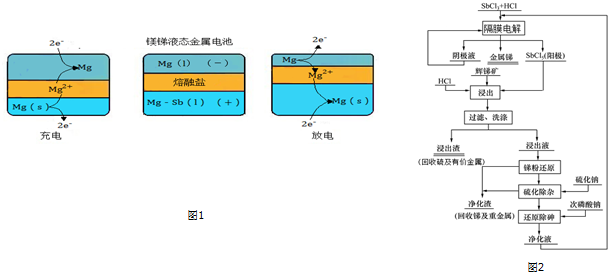
12.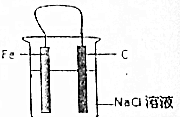 有关Fe-C-Nac1溶液构成的原电池中,叙述错误的是( )
有关Fe-C-Nac1溶液构成的原电池中,叙述错误的是( )
 有关Fe-C-Nac1溶液构成的原电池中,叙述错误的是( )
有关Fe-C-Nac1溶液构成的原电池中,叙述错误的是( )| A. | 铁片为负极,碳棒为正极 | |
| B. | 铁被腐蚀,碳棒上有氯气放出 | |
| C. | 碳棒附近的溶液可使酚酞变红 | |
| D. | 导线上有电流通过,电流方向是由碳极流向铁极 |
11.下列说法正确的( )
| A. | 苯主要是从石油分馏中获得的一种重要化工原料 | |
| B. | 甲烷和苯都能使酸性高锰酸钾溶液褪色 | |
| C. | 石油和煤均属于化石燃料,所含元素种类不相同 | |
| D. | C3H8有两种同分异构体,C5H12有三种同分异构体 |
10.很多有机反应都会受反应条件的影响,同样的反应物,如果反应条件不同,其生成物可能截然不同,下列各项中不能体现这一观点的是( )
| 反应物 | 反应条件1 | 反应条件2 | |
| A | CH3CHICH3 | NaOH的水溶液,加热 | NaOH的乙醇溶液,加热 |
| B | 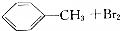 | 光照 | 铁粉 |
| C | 乙醇+氧 | 点燃 | Cu做催化剂,加热 |
| D | 乙烯 | 溴水 | 溴的四氯化碳溶液 |
| A. | A | B. | B | C. | C | D. | D |
8.某稀溶液中含有4mol KNO3和2.5mol H2SO4,向其中加入1.5mol Fe,充分反应(已知NO3-被还原为NO).下列说法正确的是( )
| A. | 反应后生成NO的体积为28 L | B. | 所得溶液中c(Fe2+):c(Fe3+)=1:1 | ||
| C. | 所得溶液中c(NO3-)=2.75 mol/L | D. | 所得溶液中的溶质只有FeSO4 |
7.向含有下列微粒的溶液中分别加入少量NaOH固体、少量浓盐酸或少量酸性高锰酸钾溶液,都能使该微粒浓度下降的是( )
| A. | Fe3+ | B. | HS- | C. | 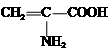 | D. | C6H5O- |
6.下列物质的熔点,前者大于后者的是( )
0 155151 155159 155165 155169 155175 155177 155181 155187 155189 155195 155201 155205 155207 155211 155217 155219 155225 155229 155231 155235 155237 155241 155243 155245 155246 155247 155249 155250 155251 155253 155255 155259 155261 155265 155267 155271 155277 155279 155285 155289 155291 155295 155301 155307 155309 155315 155319 155321 155327 155331 155337 155345 203614
| A. | 晶体硅、碳化硅 | B. | 氯化钠、甲苯 | C. | 氧化钠、氧化镁 | D. | 钾钠合金、钠 |