题目内容
10.很多有机反应都会受反应条件的影响,同样的反应物,如果反应条件不同,其生成物可能截然不同,下列各项中不能体现这一观点的是( )| 反应物 | 反应条件1 | 反应条件2 | |
| A | CH3CHICH3 | NaOH的水溶液,加热 | NaOH的乙醇溶液,加热 |
| B | 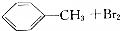 | 光照 | 铁粉 |
| C | 乙醇+氧 | 点燃 | Cu做催化剂,加热 |
| D | 乙烯 | 溴水 | 溴的四氯化碳溶液 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.NaOH的水溶液,加热条件下发生水解反应,而NaOH的乙醇溶液,加热条件下发生消去反应;
B.光照甲基上H被取代,铁粉条件下苯环上上H被取代;
C.点燃生成二氧化碳和水,催化氧化生成乙醛;
D.均发生乙烯与溴的加成反应.
解答 解:A.NaOH的水溶液,加热条件下发生水解反应,而NaOH的乙醇溶液,加热条件下发生消去反应,分别生成2-丙醇、丙烯,故A不选;
B.光照甲基上H被取代,铁粉条件下苯环上上H被取代,分别生成氯甲苯、甲基氯苯,故B不选;
C.点燃生成二氧化碳和水,催化氧化生成乙醛,条件不同产物不同,故C不选;
D.均发生乙烯与溴的加成反应,均生成1,2-二溴乙烷,故D选;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意反应条件与反应类型的关系,题目难度不大.

练习册系列答案
相关题目
20.离子方程式Ba2++2OH-+2H++SO42-→BaSO4↓+2H2O可表示( )
| A. | Ba(OH)2与NaHSO4两溶液的溶质按物质的量之比2:1反应 | |
| B. | Ba(OH)2与NaHSO4两溶液的溶质按物质的量之比1:2反应 | |
| C. | Ba(OH)2与NH4HSO4两溶液的溶质按物质的量之比2:1反应 | |
| D. | Ba(OH)2与NH4HSO4两溶液的溶质按物质的量之比1:2反应 |
1.PX是纺织工业的基础原料,其结构简式为 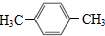 ,下列关于PX的说法正确的是( )
,下列关于PX的说法正确的是( )
 ,下列关于PX的说法正确的是( )
,下列关于PX的说法正确的是( )| A. | 属于饱和烃 | B. | 其一氯代物有四种 | ||
| C. | 可用于生产对苯二甲酸 | D. | 分子中所有原子都处于同一平面 |
18. 25℃时,向100mL 0.1mol•L-1 NH4HSO4溶液中滴加0.1mol•L-1 NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图(H2SO4视为二元强酸).下列说法错误的是( )
25℃时,向100mL 0.1mol•L-1 NH4HSO4溶液中滴加0.1mol•L-1 NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图(H2SO4视为二元强酸).下列说法错误的是( )
 25℃时,向100mL 0.1mol•L-1 NH4HSO4溶液中滴加0.1mol•L-1 NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图(H2SO4视为二元强酸).下列说法错误的是( )
25℃时,向100mL 0.1mol•L-1 NH4HSO4溶液中滴加0.1mol•L-1 NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图(H2SO4视为二元强酸).下列说法错误的是( )| A. | a点时溶液的pH<1 | |
| B. | c点时离子浓度大小顺序为:c(Na+)>c(SO42-)>c(NH4+) | |
| C. | de段上的点均满足关系式:c(NH4+)+c(Na+)>2c(SO42-) | |
| D. | a点到b点的过程中,溶液的导电能力增强 |
15.在一定条件下,反应2A(g)+B(g)?2C(g)在一密闭容器中达到平衡.充入适量B气体并维持B浓度和容器的温度不变,增大容器的体积,跟原平衡相比较达到新平衡时A的转化率将( )
| A. | 增大 | B. | 减小 | C. | 不变 | D. | 无法判断 |
2.莫尔盐,简称FAS,蓝绿色的无机复盐,在空气中逐渐风化及氧化,其名来源于德国化学家莫尔(Karl Friedrich Mohr).工业常用的制备方法是从废铁屑中回收铁屑(不含铁之外的其他金属元素),经碱溶液洗净之后,用过量硫酸溶解;再加入稍过量硫酸铵饱和溶液,在小火下蒸发溶剂直到晶膜出现,停火利用余热蒸发溶剂;过滤后用少量乙醇洗涤.莫尔盐的化学式可能是( )
| A. | NH4Fe(SO4)2•12H2O | B. | NH4Al(SO4)2•12H2O | C. | (NH4)2Fe(SO4)2•6H2O | D. | (NH4)2Fe(SO4)2 |
6.25℃和101kPa时,乙烷、乙炔和丙烯组成的混合烃32mL,与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小了72mL,原混合烃中乙炔的体积分数为( )
| A. | 12.5% | B. | 25% | C. | 50% | D. | 75% |
7.下列元素在自然界有以游离态存在的是( )
| A. | S | B. | Na | C. | Si | D. | Cl |
