1.实验室有下列试剂①浓H2S04、②稀H2S04、③稀HNO3、④浓盐酸、③含硫、磷杂质的锌粒、③纯锌、⑦CuSO4溶液,为快速制取较纯的H2,试剂的最佳选择是( )
| A. | ①⑥ | B. | ③⑤ | C. | ④⑥⑦ | D. | ②⑥⑦ |
18.恒容容器甲与恒压容器乙开始时的体积相同,均充有1molCH4和1molCO2的混合气体,发生反应:CH4(g)+CO2(g)?2CO(g)+2H2(g)△H=+247.3kJ/mol,经一段时间均达到平衡(保持温度不变).有关平衡时的下列叙述正确的是( )
| A. | 甲、乙中CO的体积分数相同 | |
| B. | 达到平衡时,甲用时间比乙短 | |
| C. | 甲中CO2的转化率比乙高 | |
| D. | 若甲、乙中都再充入同量的氦气,平衡均不移动 |
16.对下列实验的描述正确的是( )
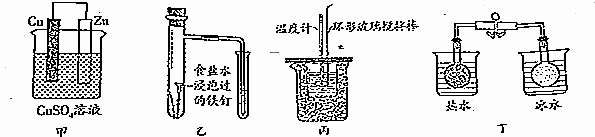

| A. | 图甲所示的实验:根据溶液颜色变化可比较Zn、Cu的金属活动性 | |
| B. | 图乙所示的实验:根据小试管中液面的变化判断铁钉发生析氢腐蚀 | |
| C. | 图丙所示的实验:根据温度计读数的变化用浓硫酸和Na0H反应测定中和热 | |
| D. | 图丁所示的实验:根据两烧瓶中气体颜色的变化判断2N02(g)?N20(g)是吸热反应 |
15.0.1mo1•L-1的CH3COOK溶液中,由于CH3COO-的水解,使得c(CH3C00-)<0.1mol•L-1.如果要使c(CH3C00-)更接近于0.1mo1•L-1,可以采取的措施是( )
| A. | 加入少量盐酸 | B. | 加入适量的水 | C. | 加入适量的KOH | D. | 加热 |
14.化学测定有机物结构的分析方法很多,下列不属于测定有机物结构的分析方法的是( )
| A. | 核磁共振 | B. | 红外光谱 | C. | 同位素示踪法 | D. | 质谱法 |
13.已知0.1mol/L的醋酸溶液中存在电离平衡:CH3COOH?CH3COO-+H+,要使溶液中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$比值增大,可以采用的措施是( )
| A. | 加少量CH3COONH4固体 | B. | 加浓醋酸 | ||
| C. | 加少量NaCl固体 | D. | 升高温度 |
12.反应4NH3+5O2?4NO+6H2O,在2L的密闭容器中进行,半分钟后,NO的物质的量增加了0.1mol,则此反应的平均反应速率表示正确的是( )
0 154683 154691 154697 154701 154707 154709 154713 154719 154721 154727 154733 154737 154739 154743 154749 154751 154757 154761 154763 154767 154769 154773 154775 154777 154778 154779 154781 154782 154783 154785 154787 154791 154793 154797 154799 154803 154809 154811 154817 154821 154823 154827 154833 154839 154841 154847 154851 154853 154859 154863 154869 154877 203614
| A. | v(NH3)=0.1mol•L-1•min-1 | B. | v(O2)=0.15mol•L-1•min-1 | ||
| C. | v(NO)=0.2mol•L-1•min-1 | D. | v(H2O)=0.25mol•L-1•min-1 |
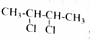 为原料制备某五元环化合物的流程如图所示:
为原料制备某五元环化合物的流程如图所示: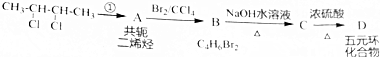
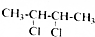 的系统命名为2,3-二氯丁烷.
的系统命名为2,3-二氯丁烷.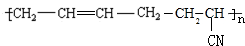 等.
等.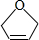 .
. N2H+5+OH-,25℃时水溶液中肼与强酸反应结合一个质子的平衡常数Kb1=$\frac{c({N}_{2}{{H}_{5}}^{+})}{c({N}_{2}{H}_{4})×c({H}^{+})}$.常温下,若将2mol/LN2H4•H20溶液与1.3mol/L硫酸溶液等体积混合,则溶液中各微粒(离子及N2H4•H2O)浓度由大到小的顺序为c(N2H5+)>c(SO4-)>c(N2H62+)>c(H+)>c(N2H4)>c(OH-).
N2H+5+OH-,25℃时水溶液中肼与强酸反应结合一个质子的平衡常数Kb1=$\frac{c({N}_{2}{{H}_{5}}^{+})}{c({N}_{2}{H}_{4})×c({H}^{+})}$.常温下,若将2mol/LN2H4•H20溶液与1.3mol/L硫酸溶液等体积混合,则溶液中各微粒(离子及N2H4•H2O)浓度由大到小的顺序为c(N2H5+)>c(SO4-)>c(N2H62+)>c(H+)>c(N2H4)>c(OH-).