题目内容
16.对下列实验的描述正确的是( )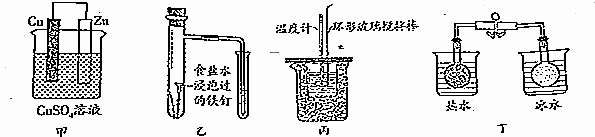
| A. | 图甲所示的实验:根据溶液颜色变化可比较Zn、Cu的金属活动性 | |
| B. | 图乙所示的实验:根据小试管中液面的变化判断铁钉发生析氢腐蚀 | |
| C. | 图丙所示的实验:根据温度计读数的变化用浓硫酸和Na0H反应测定中和热 | |
| D. | 图丁所示的实验:根据两烧瓶中气体颜色的变化判断2N02(g)?N20(g)是吸热反应 |
分析 A.Cu、Zn原电池中,活泼金属为负极;
B.在中性溶液中发生吸氧腐蚀;
C.中和热测定应选稀的强酸;
D.热水中颜色深,则逆反应为吸热反应.
解答 解:A.Cu、Zn原电池中,活泼金属为负极,则根据检流计(G)中指针偏转的方向可比较Zn、Cu的金属活泼性,故A正确;
B.析氢腐蚀生成氢气,而吸氧腐蚀中氧气得电子,气体减少,用食盐水浸泡应发生吸氧腐蚀,故B错误;
C.中和热测定应选稀的强酸,则不能利用浓硫酸测定中和热,故C错误;
D.热水中颜色深,则逆反应为吸热反应,所以正反应为放热反应,故D错误;
故选A.
点评 本题考查较综合,为高考常见题型,侧重于学生的分析、实验能力的考查,涉及原电池和电解原理、中和热测定、温度对化学平衡的影响等,注意把握实验的严密性和可行性的评价,题目难度中等.

练习册系列答案
相关题目
6.下来气体有颜色的是( )
| A. | Cl2 | B. | O2 | C. | NO | D. | CO |
11.在一定条件下,对于在密封容器中进行的反应:P(g)+Q(g)?R(g)+S(g),下列情况已经达到化学平衡状态的是( )
| A. | P、Q、R、S的浓度相等 | B. | P、Q、R、S在密闭容器中共存 | ||
| C. | P、Q、R、S的浓度不再变化 | D. | 容器内的压强不再变化 |