8.在25℃时,FeS的Ksp=6.3×10-18,CuS的Ksp=1.3×10-36,ZnS的Ksp=1.3×10-24.下列有关说法中正确的是( )
| A. | 25℃时,CuS的溶解度大于ZnS的溶解度 | |
| B. | 25℃时,向含有等物质的量的FeCl2、CuCl2的混合液中逐滴加入Na2S,最先出现沉淀的是FeS | |
| C. | 除去ZnCl2溶液中的Cu2+,可以选用FeS作沉淀剂 | |
| D. | 将足量CuSO4溶解在0.1mol/L的H2S溶液中,S2-能达到的最大浓度为$\sqrt{1.3}×{10^{-18}}mol/L$ |
6.已知某温度下,Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1×10-12.下列关于该温度下的叙述正确的是( )
| A. | 向氯化银的悬浊液中加入氯化钠溶液,Ksp(AgCl) 减小 | |
| B. | 饱和AgCl溶液与饱和Ag2CrO4溶液相比,前者的c(Ag+)大 | |
| C. | 若向0.0008 mol•L-1的K2CrO4溶液中加入等体积0.002 mol•L-1的AgNO3溶液,则CrO42-完全沉淀(提示:沉淀完全c(CrO42-)≤10-5 mol•L-1) | |
| D. | 若将0.001 mol•L-1 AgNO3溶液滴入浓度均为0.001 mol•L-1的KCl和K2CrO4混合溶液中,则先产生AgCl沉淀 |
4.根据下列流程处理废旧电路板,回收金属M,并制得高效绿色净水剂K2EO4.
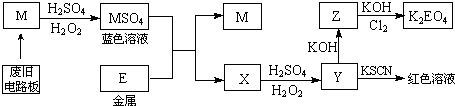
据此回答问题:
(1)M的化学式是Cu.
(2)M→MSO4过程中,氧化剂是H2O2,还原剂是Cu.
(3)写出Z→K2EO4的化学反应方程式:2Fe(OH)3+10KOH+3Cl2=2K2FeO4+8H2O+6KCl.
(4)向Y溶液中滴加KI淀粉溶液,变为蓝色,其原因用离子方程式解释为:2Fe3++2I-═2Fe2++I2.
(5)控制其他条件相同,印刷电路板的金属 M用10%H2O2和3.0mol/LH2SO4的混合溶液处理,测得不同温度下金属M的平均溶解速率(见下表).
当温度高于40℃时,M的平均溶解速率随着反应温度升高而下降,其主要原因是过氧化氢分解浓度降低造成速率减慢.

据此回答问题:
(1)M的化学式是Cu.
(2)M→MSO4过程中,氧化剂是H2O2,还原剂是Cu.
(3)写出Z→K2EO4的化学反应方程式:2Fe(OH)3+10KOH+3Cl2=2K2FeO4+8H2O+6KCl.
(4)向Y溶液中滴加KI淀粉溶液,变为蓝色,其原因用离子方程式解释为:2Fe3++2I-═2Fe2++I2.
(5)控制其他条件相同,印刷电路板的金属 M用10%H2O2和3.0mol/LH2SO4的混合溶液处理,测得不同温度下金属M的平均溶解速率(见下表).
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| V(M)(x10-3mol.L-1.min-1) | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
11.W是由短周期元素X、Y、Z组成的盐.X、Y、Z原子的最外层电子数依次增大,Z原子最外层电子数是内层电子数的3倍;X、Y原子最外层电子数之和等于Z原子的最外层电子数;Y、Z同周期且相邻,但与X不同周期.下列说法一定正确的是( )
0 154568 154576 154582 154586 154592 154594 154598 154604 154606 154612 154618 154622 154624 154628 154634 154636 154642 154646 154648 154652 154654 154658 154660 154662 154663 154664 154666 154667 154668 154670 154672 154676 154678 154682 154684 154688 154694 154696 154702 154706 154708 154712 154718 154724 154726 154732 154736 154738 154744 154748 154754 154762 203614
| A. | 三种元素的最高正化合价中,Z的最大 | |
| B. | W溶液显碱性或中性 | |
| C. | 原子半径:X>Y>Z | |
| D. | Y的最高价氧化物对应的水化物是强酸. |