3.关于阿司匹林,下列说法正确的是( )


| A. | 不能用FeCl3 溶液鉴别水杨酸和阿司匹林 | |
| B. | 服用阿司匹林出现水杨酸反应时,可静脉注射NaHCO3溶液 | |
| C. | 1 mol阿司匹林最多可消耗2 mol NaOH | |
| D. | 该反应不属于取代反应 |
2.相同状况下的12C18O和14N2两种气体,下列说法正确的是( )
| A. | 若分子数相等,则体积相等 | B. | 若原子数相等,则中子数相等 | ||
| C. | 若质量相等,则质子数相等 | D. | 若体积相等,则质量数相等 |
1.晋葛洪《抱朴子内篇•黄白》记载“曾青涂铁,铁赤色如铜”(“曾青”是指硫酸铜).下列说法不正确的是( )
| A. | 记载中的反应属于置换反应 | B. | 记载中蕴含了湿法炼铜的原理 | ||
| C. | 由记载得出铁单质是赤色(红色) | D. | 每生成1mol铜转移2mol电子 |
17. 甲图为一种新型污水处理装置,该装置可利用一种微生物将有机废水的化学能直接转化为电能.乙图是一种家用环保型消毒液发生器,用惰性电极电解饱和食盐水.下列说法中正确的是( )
甲图为一种新型污水处理装置,该装置可利用一种微生物将有机废水的化学能直接转化为电能.乙图是一种家用环保型消毒液发生器,用惰性电极电解饱和食盐水.下列说法中正确的是( )
 甲图为一种新型污水处理装置,该装置可利用一种微生物将有机废水的化学能直接转化为电能.乙图是一种家用环保型消毒液发生器,用惰性电极电解饱和食盐水.下列说法中正确的是( )
甲图为一种新型污水处理装置,该装置可利用一种微生物将有机废水的化学能直接转化为电能.乙图是一种家用环保型消毒液发生器,用惰性电极电解饱和食盐水.下列说法中正确的是( )| A. | 装置乙的b极要与装置甲的X极连接 | |
| B. | 装置乙中a极的电极反应式为2Cl--2e-═Cl2↑ | |
| C. | 若有机废水中主要含有葡萄糖,则装置甲中M的电极反应式为:C6H12O6+6H2O-24e-═6CO2↑+24H+ | |
| D. | N电极发生还原反应,当N电极消耗56 L气体(标准状况下)时,则有2NA个H+通过离子交换膜 |
16.化学与生产、生活、环境等社会实际密切相关.下列叙述错误的是( )
| A. | 减少机动车尾气的排放,可以降低雾霾的发生 | |
| B. | 垃圾焚烧法已成为许多城市垃圾处理的主要方法之一,利用垃圾焚烧产生的热能发电或供热,能较充分地利用生活垃圾中的生物质能 | |
| C. | 推广使用煤液化技术,可减少二氧化碳等温室气体的排放 | |
| D. | 燃料电池是一种高效、环境友好的发电装置 |
14. 四种常见元素的性质或结构信息如下表,试根据信息回答有关问题.
四种常见元素的性质或结构信息如下表,试根据信息回答有关问题.
(1)A元素与其同周期相邻两种元素原子的第一电离能由大到小的顺序为N>O>C(用元素符号表示);试解释其原因同周期随原子序数增大第一电离能呈增大趋势,N元素2p轨道容纳3个电子,处于半满稳定状态,能量较低,第一电离能高于同周期相邻元素,故第一电离能由大到下的顺序为N>O>C.
(2)B元素的低价氧化物分子中心原子的杂化方式为sp2,B元素的最高价氧化物分子VSEPR模型为平面三角形,B元素与D元素形成分子空间构型为直线型.
(3)D元素最高价氧化物的熔点比同主族相邻元素最高价氧化物的熔点低(填“高”或“低”),其原因是晶体类型不同,二氧化碳形成分子晶体,二氧化硅形成原子晶体.
(4)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,观察到的现象为先生成蓝色沉淀,后沉淀溶解生成深蓝色溶液;后一现象的化学反应方程式为Cu(OH)2+4NH3=[Cu(NH3)4](OH)2.
(5)某同学根据上述信息,推断A基态原子的核外电子排布为: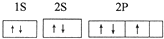
该同学所画的电子排布图违背了洪特规则.
(6)C晶体的堆积方式如图所示,设C原子半径为r cm,阿伏伽德罗常数用NA表示,则晶胞中C原子的配位数为12,C晶体的密度为$\frac{16}{\sqrt{2}{r}^{3}{N}_{A}}$g•cm-3(要求写表达式,可以不化简).
0 154478 154486 154492 154496 154502 154504 154508 154514 154516 154522 154528 154532 154534 154538 154544 154546 154552 154556 154558 154562 154564 154568 154570 154572 154573 154574 154576 154577 154578 154580 154582 154586 154588 154592 154594 154598 154604 154606 154612 154616 154618 154622 154628 154634 154636 154642 154646 154648 154654 154658 154664 154672 203614
 四种常见元素的性质或结构信息如下表,试根据信息回答有关问题.
四种常见元素的性质或结构信息如下表,试根据信息回答有关问题.| 元素 | A | B | C | D |
| 性质 结构 信息 | 原子核外有两个电子层,最外层有3个未成对的电子 | 原子的M层有1对成对的p电子 | 原子核外电子排布为[Ar]3d104sx, 有+1、+2两种常见化合价 | 有两种常见氧化物,其中有一种是冶金工业常用的还原剂 |
(2)B元素的低价氧化物分子中心原子的杂化方式为sp2,B元素的最高价氧化物分子VSEPR模型为平面三角形,B元素与D元素形成分子空间构型为直线型.
(3)D元素最高价氧化物的熔点比同主族相邻元素最高价氧化物的熔点低(填“高”或“低”),其原因是晶体类型不同,二氧化碳形成分子晶体,二氧化硅形成原子晶体.
(4)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,观察到的现象为先生成蓝色沉淀,后沉淀溶解生成深蓝色溶液;后一现象的化学反应方程式为Cu(OH)2+4NH3=[Cu(NH3)4](OH)2.
(5)某同学根据上述信息,推断A基态原子的核外电子排布为:

该同学所画的电子排布图违背了洪特规则.
(6)C晶体的堆积方式如图所示,设C原子半径为r cm,阿伏伽德罗常数用NA表示,则晶胞中C原子的配位数为12,C晶体的密度为$\frac{16}{\sqrt{2}{r}^{3}{N}_{A}}$g•cm-3(要求写表达式,可以不化简).

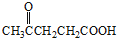 )合成聚芳酯E的路线(省略部分产物):
)合成聚芳酯E的路线(省略部分产物):
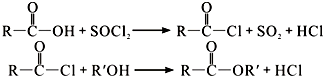
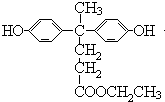
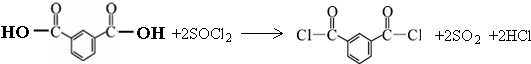 .
. 的路线.
的路线. .
.

 ;
;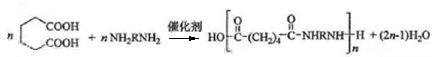 ;
; ;
; .
.