题目内容
1.晋葛洪《抱朴子内篇•黄白》记载“曾青涂铁,铁赤色如铜”(“曾青”是指硫酸铜).下列说法不正确的是( )| A. | 记载中的反应属于置换反应 | B. | 记载中蕴含了湿法炼铜的原理 | ||
| C. | 由记载得出铁单质是赤色(红色) | D. | 每生成1mol铜转移2mol电子 |
分析 根据金属活动性顺序,活动性强的金属能将活动性弱的金属从其盐溶液中置换出来.
解答 解:根据金属活动性顺序,活动性强的金属能将活动性弱的金属从其盐溶液中置换出来.由Fe+CuSO4═Cu+FeSO4可知:
A、该反应符合“单+化=单+化”的特点,属于置换反应,故A正确;
B、铁能将硫酸铜溶液中的铜元素置换出来,记载中蕴含了湿法炼铜的原理,故B正确;
C、这里的“赤色”是铜,故C错误;
D、+2价的铜离子变成单质铜,每生成1mol铜转移2mol电子,故D正确;
故选C.
点评 本题主要考查湿法冶金、金属活动性顺序、金属和盐的性质,难度较小.

练习册系列答案
相关题目
11.NA代表阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 28g乙烯中存在的电子总数为12NA | |
| B. | 标准状况下,22.4LHF的物质的量为1mol | |
| C. | 铅蓄电池电解氯化钠溶液,得到标况下22.4L氢气,理论上铅蓄电池中消耗氢离子个数为4NA | |
| D. | lmol的Na2C03溶于盐酸形成混合溶液1L,常温下在pH=4时,c(CO32- )+c(H2C03)=0.lmol/L |
12.设NA为阿伏加罗常数的值,下列说法正确的是( )
| A. | 1molMg在空气中完全燃烧生成MgO和Mg2N3,转移的电子数为NA | |
| B. | 14g分子式为CnH2n的链烃中含有的C-H键的数目为2NA | |
| C. | 室温时,1.0LpH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA | |
| D. | Fe与水蒸汽反应生成22.4L氢气,转移电子数为2NA |
9.能正确表示下列反应的离子方程式为( )
| A. | CaCl2溶液中通入CO2:Ca2++CO2+H2O═CaCO3↓+2H+ | |
| B. | 酸性KMnO4溶液中通入SO2:5SO2+2MnO4-+2H2O═5SO42-+2Mn2++4H+ | |
| C. | FeBr2溶液中通入足量Cl2:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| D. | AgCl悬浊液中通HI:Ag++HI═AgI↓+H+ |
16.化学与生产、生活、环境等社会实际密切相关.下列叙述错误的是( )
| A. | 减少机动车尾气的排放,可以降低雾霾的发生 | |
| B. | 垃圾焚烧法已成为许多城市垃圾处理的主要方法之一,利用垃圾焚烧产生的热能发电或供热,能较充分地利用生活垃圾中的生物质能 | |
| C. | 推广使用煤液化技术,可减少二氧化碳等温室气体的排放 | |
| D. | 燃料电池是一种高效、环境友好的发电装置 |
13.根据热化学方程式:S(s)+O2(g)→SO2(g)+297.23kJ,下列说法正确的是( )
| A. | 1 mol SO2 (g)的能量总和大于1 mo S(s)和1 mol O2(g)的能量总和 | |
| B. | 加入合适的催化剂,可增加单位质量的硫燃烧放出的热量 | |
| C. | S(g)+O2(g)→SO2(g)+Q1 kJ;Q1的值大于297.23 | |
| D. | 足量的硫粉与标况下1升氧气反应生成1升二氧化硫气体时放出297.23 kJ热量 |
10.如图所示下列分析错误的是( )


| A. | 只闭合K2,该装置将电能转化为化学能 | |
| B. | 只闭合K1,石墨棒周围溶液pH逐渐升高 | |
| C. | 只闭合K2,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法 | |
| D. | 铁腐蚀的速度由大到小的顺序是:只闭合K1>都断开>只闭合K2 |
11.下列液体混合物中可以用分液漏斗进行分离的是( )
| A. | 氯乙烷和水 | B. | 乙醇与水 | C. | 乙酸乙酯和乙醇 | D. | 漠苯与苯 |

 )的合成路线如下:
)的合成路线如下: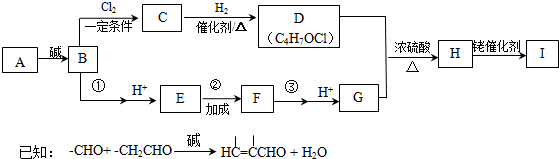
 ,B→C的反应类型为取代反应.
,B→C的反应类型为取代反应. .
.