题目内容
17. 甲图为一种新型污水处理装置,该装置可利用一种微生物将有机废水的化学能直接转化为电能.乙图是一种家用环保型消毒液发生器,用惰性电极电解饱和食盐水.下列说法中正确的是( )
甲图为一种新型污水处理装置,该装置可利用一种微生物将有机废水的化学能直接转化为电能.乙图是一种家用环保型消毒液发生器,用惰性电极电解饱和食盐水.下列说法中正确的是( )| A. | 装置乙的b极要与装置甲的X极连接 | |
| B. | 装置乙中a极的电极反应式为2Cl--2e-═Cl2↑ | |
| C. | 若有机废水中主要含有葡萄糖,则装置甲中M的电极反应式为:C6H12O6+6H2O-24e-═6CO2↑+24H+ | |
| D. | N电极发生还原反应,当N电极消耗56 L气体(标准状况下)时,则有2NA个H+通过离子交换膜 |
分析 甲为原电池,有机物失电子在负极反应,氧气得电子在正极反应;乙为电解池,在下端生成氯气,上端生成氢氧化钠和氢气,氯气与氢氧化钠反应生成次氯酸钠,则下端为阳极,所以b与正极相连.
解答 解:A、装置乙的a极上生成氢氧化钠和氢气,则a为阴极,与甲中的负极相连,即与X相连,b极要与装置甲的Y极连接,故A错误;
B、乙为电解池,在下端生成氯气,则b极的电极反应式为2Cl--2e-═Cl2↑,故B错误;
C、若有机废水中主要含有葡萄糖,则装置甲中M极上C6H12O6失电子生成二氧化碳,其电极应为:C6H12O6+6H2O-24e-═6CO2↑+24H+,故C正确;
D、N电极为氧气得电子发生还原反应,电极反应式为:O2+4H++4e-=2H2O,则当N电极消耗5.6 L气体(标准状况下)即0.25mol时,消耗的氢离子为1mol,则有NA个H+通过离子交换膜,故D错误;
故选C.
点评 本题考查了原电池原理和电解池原理的应用,涉及电极的判断和电极反应式的书写,根据正负极上得失电子再结合电解质溶液酸碱性书写电极反应式,电解质溶液酸碱性不同,其电极反应式不同,为易错点,题目难度中等.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
7.下列除去杂质的方法正确的是( )
| A. | 除去KCl溶液中的少量K2CO3:加入适量的盐酸 | |
| B. | 除去CO2中的少量HCl:通入NaOH溶液 | |
| C. | 除去NaCl溶液中的少量MgCl2:加入适量KOH溶液,过滤 | |
| D. | 除去N2中的少量O2:通过灼热的CuO粉末 |
2.相同状况下的12C18O和14N2两种气体,下列说法正确的是( )
| A. | 若分子数相等,则体积相等 | B. | 若原子数相等,则中子数相等 | ||
| C. | 若质量相等,则质子数相等 | D. | 若体积相等,则质量数相等 |
9.加入少许下列一种物质,不能使溴水颜色显著变浅的是( )
| A. | Mg粉 | B. | KOH溶液 | C. | KI溶液 | D. | CCl4 |
6.下列物质工业生产主要原理不涉及氧化还原的是( )
| A. | 纯碱 | B. | 烧碱 | C. | 盐酸 | D. | 硫酸 |
7.下列各组离子在溶液中能大量共存的是( )
| A. | Na+、OH-、S2O${\;}_{3}^{2-}$、Cl- | B. | Fe2+、K+、H+、NO${\;}_{3}^{-}$ | ||
| C. | H+、C2O${\;}_{4}^{2-}$、MnO${\;}_{4}^{-}$、SO${\;}_{4}^{2-}$ | D. | Na+、Ca2+、AlO${\;}_{2}^{-}$、HCO${\;}_{3}^{-}$ |





 .
. .
. .
. .
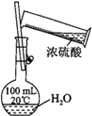
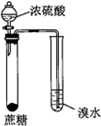
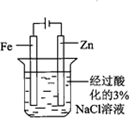
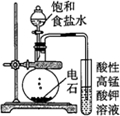
.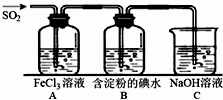 二氧化硫是硫的重要化合物,在生产、生活中有广泛应用,是大气主要污染物之一,具有一定的还原性,探究SO2气体还原Fe3+、I2,可以使用的药品和装置如图所示:
二氧化硫是硫的重要化合物,在生产、生活中有广泛应用,是大气主要污染物之一,具有一定的还原性,探究SO2气体还原Fe3+、I2,可以使用的药品和装置如图所示: