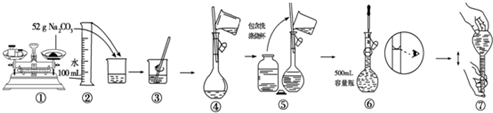
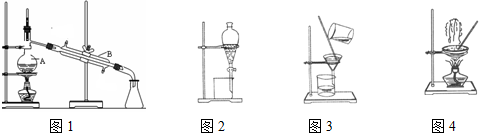
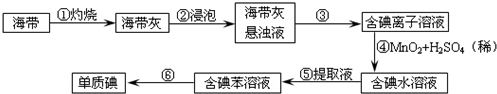
8.下列各组物质中,所含原子数相等的是( )
0 154446 154454 154460 154464 154470 154472 154476 154482 154484 154490 154496 154500 154502 154506 154512 154514 154520 154524 154526 154530 154532 154536 154538 154540 154541 154542 154544 154545 154546 154548 154550 154554 154556 154560 154562 154566 154572 154574 154580 154584 154586 154590 154596 154602 154604 154610 154614 154616 154622 154626 154632 154640 203614
| A. | 10g H2和10g O2 | B. | 标准状况下相同体积的N2和H2 | ||
| C. | 9g水和0.25mol H2 | D. | 22g CO2和3.01×1023个N2 |
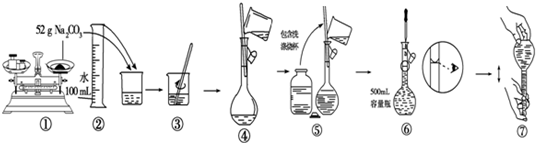
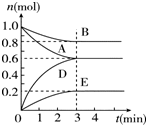 T℃、2L密闭容器中某一反应在不同时刻的各物质的量如图所示(E为固体,其余为气体).回答下列问题.
T℃、2L密闭容器中某一反应在不同时刻的各物质的量如图所示(E为固体,其余为气体).回答下列问题.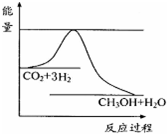 依据事实,写出下列反应的热化学方程式
依据事实,写出下列反应的热化学方程式