12.在初始温度为500℃、容积恒定为10L的三个密闭容器中,如图充料发生反应:CO2(g)+3H2(g)?CH3OH(g)十H2O(g)△H=-25k/mol.已知乙达到平衡时气体的压强为开始时的0.55倍;乙、丙中初始反应方向不同,平衡后对应各组分的体积分数相等.下列分析正确的是( )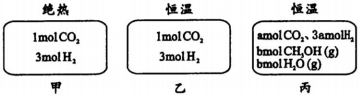

| A. | 刚开始反应时速率:甲>乙 | B. | 平衡后反应放热:甲>乙 | ||
| C. | 500℃下该反应平衡常数:K=3×102 | D. | 若a≠0,则0.9<b<l |
11. 研究人员发现了一种“水’’电池,其总反应为:5Mn02+2Ag+2NaCl=Na2Mn5O10+2AgCl.如图用“水”电池为电源电解NaCl溶液的实验中,X电极上有无色气体逸出.下列有关分析正确的是( )
研究人员发现了一种“水’’电池,其总反应为:5Mn02+2Ag+2NaCl=Na2Mn5O10+2AgCl.如图用“水”电池为电源电解NaCl溶液的实验中,X电极上有无色气体逸出.下列有关分析正确的是( )
 研究人员发现了一种“水’’电池,其总反应为:5Mn02+2Ag+2NaCl=Na2Mn5O10+2AgCl.如图用“水”电池为电源电解NaCl溶液的实验中,X电极上有无色气体逸出.下列有关分析正确的是( )
研究人员发现了一种“水’’电池,其总反应为:5Mn02+2Ag+2NaCl=Na2Mn5O10+2AgCl.如图用“水”电池为电源电解NaCl溶液的实验中,X电极上有无色气体逸出.下列有关分析正确的是( )| A. | I为负极,其电极反应式为Ag+Cl--e-=AgCl | |
| B. | “水”电池内Na+不断向负极作定向移动 | |
| C. | 每转移1mole-,U型管中消耗0.5mol H2O | |
| D. | 开始时U型管中Y极附近pH逐渐增大 |
10.下列有关0.1L 0.1mol/LKMnO4酸性溶液的叙述正确的是( )
| A. | 与少量乙二醛混合可制备乙二酸 | |
| B. | 与浓盐酸反应的离子方程式为:2MnO4-+16 H++10Cl-=5Cl2↑+2Mn2++8 H20 | |
| C. | 与K+、NO3-、SO42-、CO32-可以大量共存 | |
| D. | 与过量Na202混合后,共转移e-0.05mol |
9. 如图依次为气体制得、除杂并检验其性质的装置(加热及夹持仪器省略).下列设计不能达到目的是( )
如图依次为气体制得、除杂并检验其性质的装置(加热及夹持仪器省略).下列设计不能达到目的是( )
 如图依次为气体制得、除杂并检验其性质的装置(加热及夹持仪器省略).下列设计不能达到目的是( )
如图依次为气体制得、除杂并检验其性质的装置(加热及夹持仪器省略).下列设计不能达到目的是( )| 选项 | 气体 | 装置中药品 | ||
| a | b | C | ||
| A | C2H2 | 饱和食盐水+电石 | CuSO4溶液 | 溴水 |
| B | CO2 | 稀盐酸+石灰石 | 饱和NaHCO3溶液 | 苯酚的溶液 |
| C | C2H4 | 溴乙烷+NaOH乙醇溶液 | 水 | K2Cr2O7酸性溶液 |
| D | SO2 | 碳+浓硫酸 | 新制氯水 | 品红溶液 |
| A. | A | B. | B | C. | C | D. | D |
4.用石墨作电极电解0.1mol•L-1的NaCl溶液,通电一段时间后发现两极收集的气体体积之比为4:3,下列说法正确的是( )
| A. | 在电解后的溶液中注入一定量的盐酸可以使溶液恢复到原始状态 | |
| B. | 在电解质溶液中通入标况下4.48L的氯化氢气体并注入0.1mol的水可以使溶液恢复到原始状态 | |
| C. | 阴极产生的气体的物质的量是阳极产生气体的物质的量的0.75倍 | |
| D. | 阳极产生的气体的平均摩尔质量为58g/mol |
3.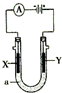 电解原理在化学工业中有广泛应用,如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.下列正确的是( )
电解原理在化学工业中有广泛应用,如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.下列正确的是( )
0 154424 154432 154438 154442 154448 154450 154454 154460 154462 154468 154474 154478 154480 154484 154490 154492 154498 154502 154504 154508 154510 154514 154516 154518 154519 154520 154522 154523 154524 154526 154528 154532 154534 154538 154540 154544 154550 154552 154558 154562 154564 154568 154574 154580 154582 154588 154592 154594 154600 154604 154610 154618 203614
 电解原理在化学工业中有广泛应用,如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.下列正确的是( )
电解原理在化学工业中有广泛应用,如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.下列正确的是( )| A. | 若X、Y为石墨,a为饱和NaCl溶液,向Y极附近加入酚酞,则Y极溶液呈红色 | |
| B. | 若X、Y是石墨,a为AgNO3溶液,电解一段时间后,溶液的pH减小 | |
| C. | 若用电解方法精炼粗铜,电解液a选用CuSO4溶液,X电极的材料是粗铜 | |
| D. | 若Y为铁,X为石墨,a为稀硫酸,Y电极反应为Fe-3e-=Fe3+ |




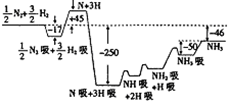 2007年度诺贝尔化学奖获得者格哈德•埃特尔建立了合成氨反应机理,T=673K时,各步反应的能量变化如图所示,图中的能量单位为kJ•mol-1.(注:图中“吸”表示在催化剂表面的吸附)请回答下列问题:
2007年度诺贝尔化学奖获得者格哈德•埃特尔建立了合成氨反应机理,T=673K时,各步反应的能量变化如图所示,图中的能量单位为kJ•mol-1.(注:图中“吸”表示在催化剂表面的吸附)请回答下列问题: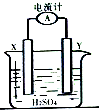 某同学进行如图所示的铜--锌原电池实验,已知电解质溶液中H+向X极移动.
某同学进行如图所示的铜--锌原电池实验,已知电解质溶液中H+向X极移动.