6.向amol/L的氨水中加入等体积b mol•L-1的盐酸,下列关系错误的是( )
| A. | 当a=b时,c(H+)=c(OH-)+c(NH3•H2O) | |
| B. | 当a>b时,c(NH4+)+c(NH3•H2O)>c(Cl-) | |
| C. | 当a<b时,c(NH4+)>c(Cl-)>c(OH-)>c(H+) | |
| D. | 当a与b为任意比时,c(NH4+)+c(H+)=c(Cl-)+c(OH-) |
5.A、B、C、D、E、F为短周期元素,且原子序数依次增大,前5种元素质子数之和为39,B、C同周期,A、D同主族,A、C能形成两种液态化合物A2C和A2C2,E元素的周期序数与主族序数相等.下列说法中不正确的是( )
| A. | 原子半径:r(D)>r(F)>r(A) | |
| B. | D与C也能形成D2C和D2C2化合物,两种化合物中阳离子和阴离子个数比都为2:1 | |
| C. | 把2mol D的单质投入足量的水中,产生的气体体积为22.4L | |
| D. | 由A、B、C三种元素组成的18电子微粒能发生氧化反应 |
4.下列离子方程式不正确的是( )
①氢氧化铜的悬浊液与盐酸反应:OH-+H+═H2O
②氯化铝溶液与过量氨水反应:Al3++3NH2•H2O═Al(OH)3↓+3NH4+
③小苏打溶液与饱和石灰水反应:HCO3-+Ca2++OH-═CaCO3↓+H2O
④苯酚钠溶液中通入过量的CO2:C6H5O-+H2O+CO2═C6H5OH↓+HCO3-.
①氢氧化铜的悬浊液与盐酸反应:OH-+H+═H2O
②氯化铝溶液与过量氨水反应:Al3++3NH2•H2O═Al(OH)3↓+3NH4+
③小苏打溶液与饱和石灰水反应:HCO3-+Ca2++OH-═CaCO3↓+H2O
④苯酚钠溶液中通入过量的CO2:C6H5O-+H2O+CO2═C6H5OH↓+HCO3-.
| A. | ①、② | B. | ①、③ | C. | ②、③ | D. | ①、④ |
1.一定温度下,对可逆反应A(g)+2B(g)?3C(g)的下列叙述中,不能说明反应已达到平衡的是( )
| A. | C生成的速率与C分解的速率相等 | |
| B. | 单位时间内消耗a mol A,同时生成3a mol C | |
| C. | 容器内的压强不再变化 | |
| D. | 混合气体中B物质的量不再变化 |
20.用标准的NaOH溶液滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏低的原因可能是( )
| A. | 滴定终点读数时,仰视滴定管的刻度,其它操作均正确 | |
| B. | 盛装未知液的滴定管用蒸馏水洗过,未用待测液润洗 | |
| C. | 滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液 | |
| D. | 未用标准液润洗碱式滴定管 |
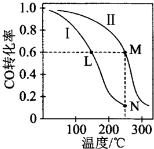
19.一定温度下,有两个体积均为2L的恒容密闭容器I和Ⅱ,向I中加入1 mol CO和2 mol H2,向Ⅱ中加入2 mol CO和4 mol H2,均发生下列反应并建立平衡:CO(g)+2H2(g)?CH3OH(g).测得不同温度下CO平衡转化率如图所示.下列说法正确的是( )
0 154363 154371 154377 154381 154387 154389 154393 154399 154401 154407 154413 154417 154419 154423 154429 154431 154437 154441 154443 154447 154449 154453 154455 154457 154458 154459 154461 154462 154463 154465 154467 154471 154473 154477 154479 154483 154489 154491 154497 154501 154503 154507 154513 154519 154521 154527 154531 154533 154539 154543 154549 154557 203614

| A. | 该反应的△H>0 | |
| B. | N点化学平衡常数K=0.59 | |
| C. | L、M两点容器内压强:P(M)>2P(L) | |
| D. | 向N点平衡体系中再加入1 mol CH3OH,建立新平衡时被分解的CH3OH物质的量小于0.4 mol |
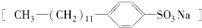 是常用洗涤剂的主要成分.其结构可用图形
是常用洗涤剂的主要成分.其结构可用图形 来表示,•端为链烃基,O端为极性基.根据这一结构特点,试分析和回答下列问题:
来表示,•端为链烃基,O端为极性基.根据这一结构特点,试分析和回答下列问题: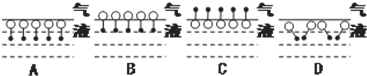
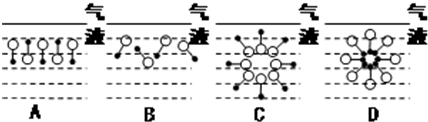
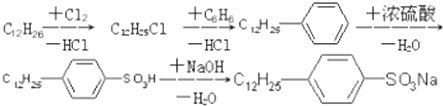
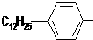 .
.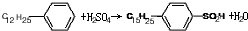 ,反应类型为取代反应.
,反应类型为取代反应.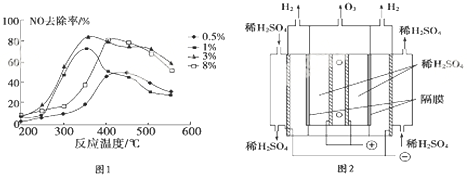
 某化学兴趣小组在实验室用如下装置制备氯气.
某化学兴趣小组在实验室用如下装置制备氯气.