题目内容
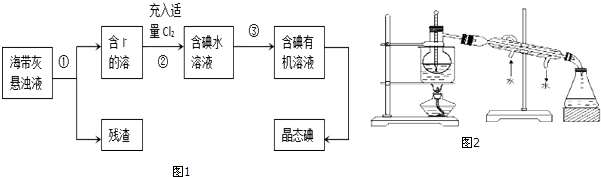
18. 某化学兴趣小组在实验室用如下装置制备氯气.
某化学兴趣小组在实验室用如下装置制备氯气.请回答:
(1)写出A装置中制取氧气的化学方程式:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(2)若要制备纯净、干燥的氯气,需在A、B之间添加净化装置D、E,其中导管连接的顺序是③④②①(填写数字编号).
分析 (1)实验室用二氧化锰与浓盐酸反应制备氯气;
(2)制备的氯气中含水蒸气、氯化氢杂质气体,制备纯净、干燥的氯气需要通过饱和食盐水除去氯化氢,通过浓硫酸除去水蒸气,导气管长进短出;
解答 解:(1)A.二氧化锰与浓盐酸反应生成氯化锰、水、氯气,方程式为:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(2)制备的氯气中含水蒸气、氯化氢杂质气体,制备纯净、干燥的氯气需要通过饱和食盐水除去氯化氢,通过浓硫酸除去水蒸气,导气管长进短出,在A、B之间添加净化装置D、E,其中导管连接的顺序是③④②①,氯气有毒,不能排放到空气中会污染空气,实验装置用氢氧化钠溶液吸收装置吸收.
故答案为:③④②①.
点评 本题考查了氯气的制备和性质的检验,主要是气体除杂的试剂选择和仪器连接,题目难度不大.

练习册系列答案
相关题目
8.下列关于NH4Fe(SO4)2溶液中离子浓度关系的说法中正确的是( )
| A. | 2c(SO42-)+c(OH-)=c(NH4+)+3c(Fe3+)+c(H+) | B. | c(NH4+)=c(Fe3+) | ||
| C. | c(NH4+)=$\frac{1}{2}$c(SO42-) | D. | c(OH-)>c(H+) |
9.某硝酸盐R(NO3)2受热分解为RO、NO2、O2,在标准状况下,将生成的气体充满一烧瓶,并将烧瓶倒置于水中,当烧瓶中液面不再上升时烧瓶内溶液浓度是( )
| A. | $\frac{4}{5}$mol•L-1 | B. | $\frac{1}{14}$mol•L-1 | C. | $\frac{1}{22.4}$mol•L-1 | D. | $\frac{1}{28}$mol•L-1 |
6.己知反应:①PbO2+4HCI═PbCl2+C12↑+2H20,②Cu+2Fe3+═Cu2++2Fe2+,③Cl2+2Fe2+═2Cl-+2Fe3+.则有关物质(离子)的氧化性由强到弱的顺序为( )
| A. | Cl2>Fe3+>Cu2+>PbO2 | B. | PbO2>Cl2>Fe3+>Cu2+ | ||
| C. | Fe3+>Cu2+>PbO2>Cl2 | D. | Cu2+>Fe3+>Cl2>PbO2 |
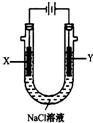
10.用石墨电极电解下列物质的水溶液,两极都有气体生成且电解过程中溶液PH增大的是( )
| A. | KI | B. | H2SO4 | C. | NaOH | D. | Na2SO4 |
 甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455kJ/mol,甲醚可作燃料电池的燃料.
甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455kJ/mol,甲醚可作燃料电池的燃料.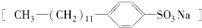 是常用洗涤剂的主要成分.其结构可用图形
是常用洗涤剂的主要成分.其结构可用图形 来表示,•端为链烃基,O端为极性基.根据这一结构特点,试分析和回答下列问题:
来表示,•端为链烃基,O端为极性基.根据这一结构特点,试分析和回答下列问题: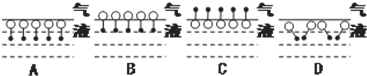
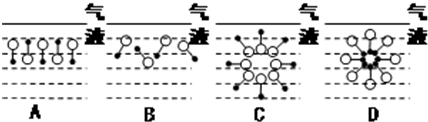
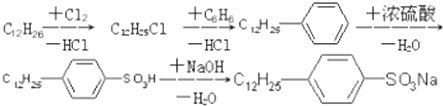
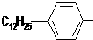 .
.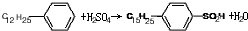 ,反应类型为取代反应.
,反应类型为取代反应.