题目内容
5.A、B、C、D、E、F为短周期元素,且原子序数依次增大,前5种元素质子数之和为39,B、C同周期,A、D同主族,A、C能形成两种液态化合物A2C和A2C2,E元素的周期序数与主族序数相等.下列说法中不正确的是( )| A. | 原子半径:r(D)>r(F)>r(A) | |
| B. | D与C也能形成D2C和D2C2化合物,两种化合物中阳离子和阴离子个数比都为2:1 | |
| C. | 把2mol D的单质投入足量的水中,产生的气体体积为22.4L | |
| D. | 由A、B、C三种元素组成的18电子微粒能发生氧化反应 |
分析 A、C能形成两种液态化合物A2C和A2C2,该液态化合物分别为H2O和H2O2,则A为H元素,C为O元素;A、D同主族,则D为Na元素;E元素的周期序数与主族序数相等,应为第三周期,处于ⅢA族元素,故E为Al元素;A、B、C、D、E为短周期元素,且原子序数依次增大,质子数之和为39,设B的原子序数为x,则有1+x+8+11+13=39,x=6,所以B为碳元素,结合元素对应的单质、化合物的性质可解答该题.
解答 解:A、C能形成两种液态化合物A2C和A2C2,该液态化合物分别为H2O和H2O2,则A为H元素,C为O元素;A、D同主族,则D为Na元素;E元素的周期序数与主族序数相等,应为第三周期,处于ⅢA族元素,故E为Al元素;A、B、C、D、E为短周期元素,且原子序数依次增大,质子数之和为39,设B的原子序数为x,则有1+x+8+11+13=39,x=6,所以B为碳元素,
A.D为Na,为短周期原子半径最大的元素,H为原子半径最小的元素,故A正确;
B.Na2O2由钠离子与过氧根离子(O22-)构成,阳离子和阴离子个数比为2:1,Na2O中阳离子和阴离子个数比也为2:1,故B正确;
C.气体存在的条件未知,不能确定体积,故C错误;
D.由A、B、C三种元素组成的18电子微粒可为CH3OH,为甲醇,可发生氧化还原反应,故D正确.
故选C.
点评 本题考查结构位置性质关系、元素周期表的结构、元素周期律等,为高频考点,侧重学生的分析能力的考查,难度不大,注意掌握元素周期律.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.下列化合物中含有手性碳原子的是( )
| A. | CCl2F2 | B. | 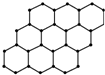 | C. | CH3CH2OH | D. | 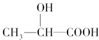 |
16.下列有关说法正确的是( )
| A. | 氨水稀释后,溶液中 的值减小 的值减小 | |
| B. | 0.1mol•L-1Na2CO3溶液加蒸馏水稀释,CO32-的水解程度增大,溶液的pH减小 | |
| C. | 电解精炼铜过程中,阳极质最的减少与阴极质量的增加一定相等 | |
| D. | 298K时,2H2S(g)+SO2(g)=3S(s)+2H2O(l)能自发进行,则其△H<0 |
20.用标准的NaOH溶液滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏低的原因可能是( )
| A. | 滴定终点读数时,仰视滴定管的刻度,其它操作均正确 | |
| B. | 盛装未知液的滴定管用蒸馏水洗过,未用待测液润洗 | |
| C. | 滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液 | |
| D. | 未用标准液润洗碱式滴定管 |
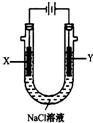
10.用石墨电极电解下列物质的水溶液,两极都有气体生成且电解过程中溶液PH增大的是( )
| A. | KI | B. | H2SO4 | C. | NaOH | D. | Na2SO4 |
17.部分弱电解质的电离平衡常数如下表,下列说法不正确的是( )
| 弱电解质 | HCOOH | HCN | H2CO3 | NH3•H2O |
| 电离平衡常数 (25℃) | Ka=1.8×10-4 | Ka=4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Kb=1.8×10-5 |
| A. | 25℃时,若将pH=3的盐酸与pH=11的氨水混合后溶液显中性,则二者消耗的体积是:V(盐酸)>V(氨水) | |
| B. | 0.1mol/L的HCOONH4溶液中:c(HCOO-)>c(NH4+)>c(H+)>c(OH-) | |
| C. | 结合H+的能力:CO32->HCO3->CN->HCOO- | |
| D. | 0.1mol/L的NaHCO3溶液中:c(H2CO3)+c(H+)=c(OH-)+c(CO32-) |
15.下列物质属于离子化合物的是( )
| A. | HCl | B. | NH3•H2O | C. | (NH4)2SO4 | D. | CH3COOH |
 甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455kJ/mol,甲醚可作燃料电池的燃料.
甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455kJ/mol,甲醚可作燃料电池的燃料. .
.