8.2006年夏季,云南的某些湖泊发生水华现象,其原因是水体出现富营养化,使某些藻类迅速繁殖,导致水生生态系统的破坏.下列选项中能够使水体富营养化的物质是( )
| A. | 含氮、磷的化合物 | B. | 含氯的化合物 | C. | 含硫的化合物 | D. | 含碳的化合物 |
7. 美国圣路易斯大学研制了一种新型的乙醇电池,其反应为:C2H5OH+3O2→2CO2+3H2O,电池示意如图,下列说法正确的是( )
美国圣路易斯大学研制了一种新型的乙醇电池,其反应为:C2H5OH+3O2→2CO2+3H2O,电池示意如图,下列说法正确的是( )
 美国圣路易斯大学研制了一种新型的乙醇电池,其反应为:C2H5OH+3O2→2CO2+3H2O,电池示意如图,下列说法正确的是( )
美国圣路易斯大学研制了一种新型的乙醇电池,其反应为:C2H5OH+3O2→2CO2+3H2O,电池示意如图,下列说法正确的是( )| A. | a极为电池的正极 | |
| B. | b极发生氧化反应 | |
| C. | 负极的反应为:4H++O2+4e-═2H2O | |
| D. | 电池工作时,1mol乙醇被氧化时有12mol转移 |
6.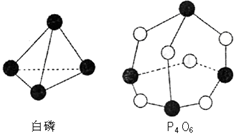 化学反应可视为旧健断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量.已知白磷和P4O6的分子结构如右图所示,现提供以下化学键的键能(kJ•mol-1)P-P:198;P-O:360;O-O:498.则反应P4(白磷)+3O2=P4O6的反应热△H为( )
化学反应可视为旧健断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量.已知白磷和P4O6的分子结构如右图所示,现提供以下化学键的键能(kJ•mol-1)P-P:198;P-O:360;O-O:498.则反应P4(白磷)+3O2=P4O6的反应热△H为( )
 化学反应可视为旧健断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量.已知白磷和P4O6的分子结构如右图所示,现提供以下化学键的键能(kJ•mol-1)P-P:198;P-O:360;O-O:498.则反应P4(白磷)+3O2=P4O6的反应热△H为( )
化学反应可视为旧健断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量.已知白磷和P4O6的分子结构如右图所示,现提供以下化学键的键能(kJ•mol-1)P-P:198;P-O:360;O-O:498.则反应P4(白磷)+3O2=P4O6的反应热△H为( )| A. | -1638kJ/mol | B. | +1638kJ/mol | C. | -126kJ/mol | D. | +126kJ/mol |
1.下列物质中,既含有极性键,又含有非极性键的是( )
| A. | 苯(C6H6) | B. | CO2 | C. | Na2O2 | D. | NH4Cl |
20.若NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A. | NA个Cl2在常温常压下体积约为22.4L | |
| B. | 在20℃、101kPa时,22.4L氢气中约含有2NA个氢原子 | |
| C. | 25℃、1.01×105Pa,48g SO2中含有的原子数为3NA | |
| D. | 22 g二氧化碳与标准状况下11.2LHCl含有相同的分子数 |
19.向紫色石蕊试液中加入过量的过氧化钠粉末,振荡,正确的叙述是( )
0 154263 154271 154277 154281 154287 154289 154293 154299 154301 154307 154313 154317 154319 154323 154329 154331 154337 154341 154343 154347 154349 154353 154355 154357 154358 154359 154361 154362 154363 154365 154367 154371 154373 154377 154379 154383 154389 154391 154397 154401 154403 154407 154413 154419 154421 154427 154431 154433 154439 154443 154449 154457 203614
| A. | 溶液为紫色 | B. | 最后溶液变为蓝色 | ||
| C. | 最后溶液褪色 | D. | 有气泡产生 |
 ;D在元素周期表中的位置为第三周期ⅢA族.
;D在元素周期表中的位置为第三周期ⅢA族.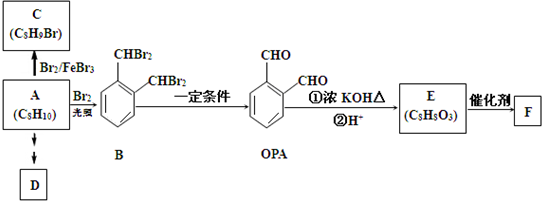

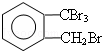 ;
; ;
; .
.
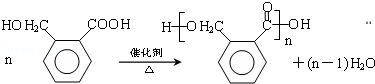 .
. .
.