12.我国古代发明或技术应用中,其工作原理不涉及化学反应的是
①指南针②黑火药③转轮排字④黏土制陶瓷⑤用玻璃瓶盛装“强水”(古书中记载一种能腐蚀五金的液体⑥用明矾溶液清洗铜镜表面的铜锈⑦湿法炼铜( )
①指南针②黑火药③转轮排字④黏土制陶瓷⑤用玻璃瓶盛装“强水”(古书中记载一种能腐蚀五金的液体⑥用明矾溶液清洗铜镜表面的铜锈⑦湿法炼铜( )
| A. | ①③④⑤ | B. | ①③⑤ | C. | ①③④⑦ | D. | ①③⑤⑥ |
9.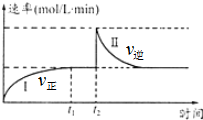 在一定恒温体积可变的密闭容器中发生如下反应:A(g)+B(g)?2C(g)△H<0.t1时刻达到平衡后,在t2时刻改变某一条件达新平衡,其反应过程如图.下列说法中错误的是(
在一定恒温体积可变的密闭容器中发生如下反应:A(g)+B(g)?2C(g)△H<0.t1时刻达到平衡后,在t2时刻改变某一条件达新平衡,其反应过程如图.下列说法中错误的是(
 在一定恒温体积可变的密闭容器中发生如下反应:A(g)+B(g)?2C(g)△H<0.t1时刻达到平衡后,在t2时刻改变某一条件达新平衡,其反应过程如图.下列说法中错误的是(
在一定恒温体积可变的密闭容器中发生如下反应:A(g)+B(g)?2C(g)△H<0.t1时刻达到平衡后,在t2时刻改变某一条件达新平衡,其反应过程如图.下列说法中错误的是(| A. | 0~t2时,v正>v逆 | |
| B. | t2时刻改变的条件可能是加催化剂 | |
| C. | Ⅰ、Ⅱ两过程达到平衡时,A的体积分数Ⅰ>Ⅱ | |
| D. | Ⅰ、Ⅱ两过程达到平衡时,平衡常数I<Ⅱ |
8.设NA为阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 3.4g H2O2中含有的共用电子对数为0.1NA | |
| B. | 25℃,pH=13的NaOH溶液中,含有OH-的数目为0.1NA | |
| C. | 标准状况下,2.24L氯气溶于水发生反应,转移的电子数目为0.1 NA | |
| D. | 标况下,11.2 L由CH4和C2H4组成的混合气体中含有氢原子的数目为2 NA |
7.下列有关原子结构、元素性质的说法正确的是( )
| A. | Si、P、S、Cl元素的单质与氢气化合越来越容易 | |
| B. | 非金属元素的非金属性越强,其氧化物对应水化物的酸性也一定越强 | |
| C. | 元素原子最外层电子数越多,元素金属性越强 | |
| D. | F-、O2-、Mg2+、Na+离子半径逐渐减小 |
6.下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:Ar(填具体元素符号,下同).
(2)NH4H电子式是: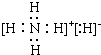 ;
;
(3)表示①与⑦的化合物的结构式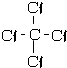 ;
;
(4)写出 ⑥的原子结构示意图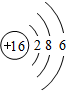 ;
;
(5)③气态氢化物的沸点大于(填“大于”、“小于”)⑥的气态氢化物的沸点.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(2)NH4H电子式是:
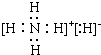 ;
;(3)表示①与⑦的化合物的结构式
 ;
;(4)写出 ⑥的原子结构示意图
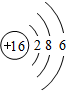 ;
;(5)③气态氢化物的沸点大于(填“大于”、“小于”)⑥的气态氢化物的沸点.
5.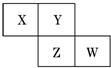 X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
 X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )| A. | X的最常见气态氢化物的水溶液显酸性 | |
| B. | 最高价氧化物对应水化物的酸性W比Z强 | |
| C. | Z的单质与氢气反应比Y单质与氢气反应剧烈 | |
| D. | X的原子半径小于Y |
4.(1)某学生为了探究铝与盐酸反应过程中的速率变化,他用排水集气法收集反应放出的氢气,实验记录如下:
①哪一时间段(即0~1、1~2、2~3、3~4、4~5min)反应速率最大2~3min,原因是因该反应是放热反应,此时温度高.
②哪一段时段的反应速率最小4~5 min,原因是此时H+浓度小.
(2)另一学生也做同样的实验,由于反应太快,不好控制测量氢气的体积,他事先在盐酸中加入等体积的下列溶液:A、蒸馏水 B、CuCl2溶液 C、NaNO3溶液,以减慢反应速率,你认为可行的是A,不可行的是BC,不可行的理由是加入少量CuCl2晶体时,CuCl2会与锌反应置换出铜,Al、铜与酸会形成原电池,发生原电池反应而加快反应速率;加入硝酸钠溶液时,存在的硝酸根离子和氢离子相当于存在硝酸,金属铝和硝酸反应不会产生氢气..
(3)下列各分子中,所有原子都满足最外层为8电子结构的是③④⑥⑦
①H2O ②BF3 ③CCl4 ④PCl3 ⑤SO3 ⑥N2 ⑦CO2.
0 154225 154233 154239 154243 154249 154251 154255 154261 154263 154269 154275 154279 154281 154285 154291 154293 154299 154303 154305 154309 154311 154315 154317 154319 154320 154321 154323 154324 154325 154327 154329 154333 154335 154339 154341 154345 154351 154353 154359 154363 154365 154369 154375 154381 154383 154389 154393 154395 154401 154405 154411 154419 203614
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 150 | 300 | 380 | 410 |
②哪一段时段的反应速率最小4~5 min,原因是此时H+浓度小.
(2)另一学生也做同样的实验,由于反应太快,不好控制测量氢气的体积,他事先在盐酸中加入等体积的下列溶液:A、蒸馏水 B、CuCl2溶液 C、NaNO3溶液,以减慢反应速率,你认为可行的是A,不可行的是BC,不可行的理由是加入少量CuCl2晶体时,CuCl2会与锌反应置换出铜,Al、铜与酸会形成原电池,发生原电池反应而加快反应速率;加入硝酸钠溶液时,存在的硝酸根离子和氢离子相当于存在硝酸,金属铝和硝酸反应不会产生氢气..
(3)下列各分子中,所有原子都满足最外层为8电子结构的是③④⑥⑦
①H2O ②BF3 ③CCl4 ④PCl3 ⑤SO3 ⑥N2 ⑦CO2.



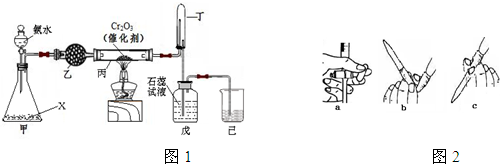

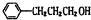 $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$ +H2O;该反应的反应类型为酯化反应或取代反应
+H2O;该反应的反应类型为酯化反应或取代反应 .
.