题目内容
7.下列有关原子结构、元素性质的说法正确的是( )| A. | Si、P、S、Cl元素的单质与氢气化合越来越容易 | |
| B. | 非金属元素的非金属性越强,其氧化物对应水化物的酸性也一定越强 | |
| C. | 元素原子最外层电子数越多,元素金属性越强 | |
| D. | F-、O2-、Mg2+、Na+离子半径逐渐减小 |
分析 A.非金属元素的非金属性越强,其氢化物越稳定;
B.非金属性越强,则最高价含氧酸的酸性越强;
C.同周期元素,原子最外层电子数越多,非金属性越强;
D.电子数相同,质子数越大,半径越小.
解答 解:A.Si、P、S、Cl为同周期元素非金属性依次增强,所以单质与氢气化合越来越容易,故A正确;
B.非金属性与最高价含氧酸的酸性成正比,即非金属性越强,则最高价氧化物对应水化物的酸性越强,故B错误;
C.同周期元素,原子最外层电子数越多,非金属性越强,不是同周期最外层电子数多非金属性不一定强,如O的非金属性大于Cl,但是Cl的最外层电子数比O多,故C错误;
D.O2-、F-、Mg2+、Na+离子具有相同的电子数,离子半径O2-、F-、Na+、Mg2+逐渐减小,故D错误;
故选A.
点评 本题考查了物质的结构、元素性质,熟悉原子结构、元素周期表结构、元素性质的递变规律是解题关键,题目难度不大,侧重于考查学生的分析能力.

练习册系列答案
相关题目
18.常温下,下列溶液中的微粒浓度关系正确的是( )
| A. | 在Na2CO3溶液中一定有:c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3) | |
| B. | 在NaHCO3溶液中一定有:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) | |
| C. | 在NH4Cl溶液中一定有:c(H+)=c(NH3•H2O)+c(OH-) | |
| D. | 在CH3COONa溶液中一定有:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
15.下列各表述与示意图一致的是( )


| A. | 图①表示向含Mg2+、Al3+、NH4+的盐溶液中滴加NaOH溶液时,沉淀的量与NaOH的体积的关系图.则三种离子的物质的量之比为:n(Mg2+):n(Al3+):n( NH4+)=2:3:2 | |
| B. | 图①中使用的NaOH的浓度为2 mol/L | |
| C. | 图②表示25℃时,用0.1 mol•L-1盐酸滴定20 mL 0.1 mol•L-1 NaOH溶液,溶液的pH随加入酸体积的变化 | |
| D. | 图③中曲线表示3H2(g)+N2(g)═2NH3(g)反应过程的能量变化.若使用催化剂,B点会降低 |
2.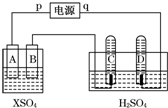 如图,p、q为直流电源两极,A为+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D产生气泡.试回答:
如图,p、q为直流电源两极,A为+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D产生气泡.试回答:
(1)p为正极,A极发生了氧化反应.
(2)左侧装置在工业上的应用电镀或粗铜精炼(写出一个即可).
(3)C为阳极,C极的电极反应式是4OH--4e-=O2↑+2H2O.
(4)在电解过程中,测得的C、D两极上产生的气体的实验数据如下:
仔细分析以上实验数据,请说出可能的原因是开始时C、D两极气体体积比为1:3,10分钟时约为1:2,说明开始时氧气溶解于溶液中.
(5)当反应进行一段时间后,A、B电极附近溶液的pH不变(填“增大”“减小”或“不变”).
(6)当电路中通过0.004mol电子时,B电极上沉积金属X为0.128g,则此金属的摩尔质量为64 g/mol.
 如图,p、q为直流电源两极,A为+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D产生气泡.试回答:
如图,p、q为直流电源两极,A为+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D产生气泡.试回答:(1)p为正极,A极发生了氧化反应.
(2)左侧装置在工业上的应用电镀或粗铜精炼(写出一个即可).
(3)C为阳极,C极的电极反应式是4OH--4e-=O2↑+2H2O.
(4)在电解过程中,测得的C、D两极上产生的气体的实验数据如下:
| 时间(min) | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 阴极生成气体 体积(cm3) | 6 | 12 | 20 | 29 | 39 | 49 | 59 | 69 | 79 | 89 |
| 阳极生成气体 | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 | 36 | 41 |
| 体积(cm3) |
(5)当反应进行一段时间后,A、B电极附近溶液的pH不变(填“增大”“减小”或“不变”).
(6)当电路中通过0.004mol电子时,B电极上沉积金属X为0.128g,则此金属的摩尔质量为64 g/mol.



 合理膳食、合理用药是人体健康的需要.
合理膳食、合理用药是人体健康的需要.