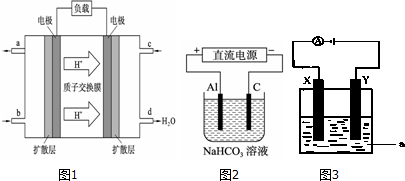
7.二氧化锰是制造锌锰干电池的基本材料.工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如图1:
某软锰矿的主要成分为MnO2,还含有Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH如表,回答下列问题
(1)硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要反应的化学方程式为MnO2+2FeSO4+2H2SO4═MnSO4+Fe2(SO4)3+2H2O.
(2)滤渣A的主要成分是SiO2;滤渣B的主要成分是Fe(OH)3、Al(OH)3.
(3)加入MnS的目的是除去Cu2+、Zn2+杂质.可能原因是CuS、ZnS的溶解度较MnS小.
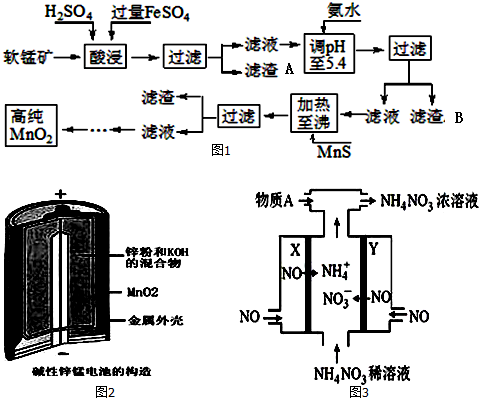
(4)碱性锌锰电池是一种一次性电池,其结构如图2所示.该电池放电过程产生MnOOH.该电池的正极反应式为MnO2+H2O+e-═MnO(OH)+OH-,电池总反应的方程式为Zn+2MnO2+2H2O═2MnOOH+ZnOH)2.
(5)利用该碱性锌锰电池电解NO制备NH4NO3,其工作原理如图3所示,X电极阴极,电解时阳极的电极反应为NO-3e-+2H2O=NO3-+4H+,使电解产物全部转化为NH4NO3,需补充物质A,A是NH3.

某软锰矿的主要成分为MnO2,还含有Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH如表,回答下列问题
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 | Zn(OH)2 | CuS | ZnS | MnS | FeS |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 | 8.0 | ≥-0.42 | ≥2.5 | ≥7 | ≥7 |
(2)滤渣A的主要成分是SiO2;滤渣B的主要成分是Fe(OH)3、Al(OH)3.
(3)加入MnS的目的是除去Cu2+、Zn2+杂质.可能原因是CuS、ZnS的溶解度较MnS小.
(4)碱性锌锰电池是一种一次性电池,其结构如图2所示.该电池放电过程产生MnOOH.该电池的正极反应式为MnO2+H2O+e-═MnO(OH)+OH-,电池总反应的方程式为Zn+2MnO2+2H2O═2MnOOH+ZnOH)2.
(5)利用该碱性锌锰电池电解NO制备NH4NO3,其工作原理如图3所示,X电极阴极,电解时阳极的电极反应为NO-3e-+2H2O=NO3-+4H+,使电解产物全部转化为NH4NO3,需补充物质A,A是NH3.
20.设NA表示阿伏加德罗常数的值,下列说法不正确的是( )
| A. | 1mol NH4+和1mol OH-所含电子数均为10NA | |
| B. | 14gC2H4和14gC3H6 所含原子数均为3NA | |
| C. | 1L l mol/LH2SO4溶液与足量Zn充分反应生成22.4L H2 | |
| D. | 标准状况下,11.2LSO3所含分子数为0.5NA |
19.下列试剂的保存方法,错误的是( )
0 154194 154202 154208 154212 154218 154220 154224 154230 154232 154238 154244 154248 154250 154254 154260 154262 154268 154272 154274 154278 154280 154284 154286 154288 154289 154290 154292 154293 154294 154296 154298 154302 154304 154308 154310 154314 154320 154322 154328 154332 154334 154338 154344 154350 154352 154358 154362 154364 154370 154374 154380 154388 203614
| A. | 把浓硝酸放在棕色瓶中,并置于冷暗处保存 | |
| B. | 把Na保存在煤油中 | |
| C. | 把NaOH溶液放在带橡皮塞的玻璃瓶中 | |
| D. | 把氢氟酸放在玻璃瓶中 |
 盐酸、硫酸和硝酸是中学阶段常见的“三大酸”.现就硫酸、硝酸与金属铜反应的情况,回答下列问题:
盐酸、硫酸和硝酸是中学阶段常见的“三大酸”.现就硫酸、硝酸与金属铜反应的情况,回答下列问题: