题目内容
3.NaCl在生活、生产和科研中都有广泛的用途.I.从海水中提取的粗盐含有Ca2+、Mg2+、SO42-等离子,为制备精盐可使用以下四种试剂:①Na2CO3溶液②BaCl2溶液③NaOH溶液④盐酸(用于沉淀的试剂均稍过量).
加入试剂的合理顺序是cd(填选项).
a.①②③④b.③①②④C.②①③④d.③②①④
II.实验室要配制100mL 0.2mol/L NaCl溶液.
(1)用托盘天平称氯化钠固体的质量是1.2g.
(2)配制溶液需要使用的主要玻璃仪器有烧杯、玻璃棒、胶头滴管和100mL容量瓶.
(3)下列操作中,可能造成所配制溶液的浓度偏低的是a (填选项)
a.没有洗涤烧杯和玻璃棒 b.定容时,俯视刻度线
c.洗涤后的容量瓶中残留少量蒸馏水.
分析 Ⅰ.(1)根据根据SO42-、Ca 2+、Mg2+等易转化为沉淀而被除去,以及根据不能产生新杂质的要求排序,前面加入的过量溶液应用后加入的溶液除去,最后加入适量的盐酸溶液;
Ⅱ.(1)根据100mL 0.2mol•L-1 NaCl溶液中含有的溶质的物质的量计算出氯化钠的质量,注意托盘天平的准确度为0.1g;
(2)根据配制一定物质的量浓度溶液的步骤选择使用的仪器;
(3)根据实验操作对物质的量浓度c=$\frac{n}{V}$中溶质的物质的量n、溶液的体积V的影响分析产生的误差情况.
解答 解:Ⅰ(1)SO42-、Ca2+、Mg2+等分别与BaCl2溶液、Na2CO3溶液、NaOH溶液反应生成沉淀,可再通过过滤除去,Na2CO3溶液能除去过量的BaCl2溶液,盐酸能除去过量的Na2CO3溶液和NaOH溶液,所以应先加BaCl2溶液再加Na2CO3溶液,最后加入盐酸,所以正确顺序为:②①③④或③②①④,
故选cd;
Ⅱ(1)100mL 0.2mol•L-1 NaCl溶液中含有氯化钠的物质的量为:0.2mol•L-1×0.1L=0.02mol,需要氯化钠的质量为:58.5g/mol×0.02mol=1.17g,由于天平只能读到0.1g,所以应该称量1.2g氯化钠,
故答案为:1.2;
(2)配制100mL 0.2mol•L-1 NaCl溶液的步骤为:计算、称量、溶解、转移、洗涤、定容、摇匀等,需要的仪器有:托盘天平、药匙、烧杯、玻璃棒、100mL容量瓶、胶头滴管,主要玻璃仪器有烧杯、玻璃棒、胶头滴管和100 mL容量瓶,
故答案为:100 mL容量瓶;
(3)a.没有洗涤烧杯和玻璃棒,导致配制的溶液中溶质读到物质的量减小,溶液得到浓度偏小,故a正确;
b.定容时,俯视刻度线,导致加入的蒸馏水体积偏小,溶液体积偏小,配制的溶液浓度偏高,故b错误;
c.洗涤后的容量瓶中残留少量蒸馏水,由于定容时还需要加入蒸馏水,所以不影响配制结果,故c错误;
故选a.
点评 本题考查了粗盐的提纯和配制一定物质的量浓度的溶液,题目难度不大,注意在除去多种杂质时,要考虑加入试剂的顺序,注意掌握配制一定物质的量浓度的溶液的配制方法.

 阅读快车系列答案
阅读快车系列答案| A. | 标准状况下,11.2LHCl和11.2LNH3充分混合后含有的分子数为NA | |
| B. | 0.1mol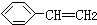 中含有碳碳双键的数目为0.4NA 中含有碳碳双键的数目为0.4NA | |
| C. | 常温常压下,1molNO2与水反应后,溶液中NO3-的数目为NA | |
| D. | 1molMg与足量空气反应生成MgO和Mg3N2,失去的电子数为2NA |
①在原溶液中滴加足量氯水后,有气泡产生,溶液呈橙黄色;
②向呈橙黄色的溶液中滴加BaCl2时无沉淀生成;
③橙黄色溶液不能使淀粉变蓝.则上述溶液中一定不存在的离子是( )
| A. | NH4+、Br-、CO32- | B. | NH4+、I-、SO32- | C. | Fe2+、I-、SO32- | D. | Fe2+、Br-、CO32- |
| A. | 升高温度,KW增大,pH变小 | |
| B. | 向水中加入氨水,平衡向逆反应方向移动,c(OH-)降低 | |
| C. | 向水中加入少量硫酸,c(H+)增大,KW变小 | |
| D. | 向水中加入少量固体CH3COONa,平衡向逆反应方向移动,c(H+)降低 |
| A. | 在NaHS溶液中滴入少量的CuCl2溶液产生黑色沉淀,HS-电离程度增大,反应后溶液pH减小 | |
| B. | 浑浊的苯酚试液中加入饱和Na2CO3溶液变澄清,则酸性:苯酚>碳酸 | |
| C. | 在等浓度NaCl和Na2CrO4稀溶液中滴加AgNO3溶液,先析出AgCl,则Ksp(AgCl)<Ksp(Ag2CrO4) | |
| D. | 等体积、物质的量浓度的HA与NaA(HA为弱酸)混合溶液,其酸碱性取决于Ka(HA)的大小 |