4.下列图象不能正确表示相关反应中产物物质的量的变化的是(横、纵坐标单位:mol)( )
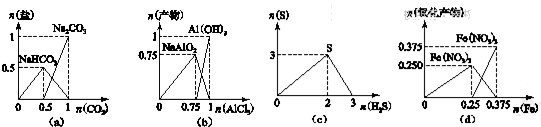

| A. | 图(a):n(NaOH)═1 mol时,CO2和NaOH溶液反应生成的盐 | |
| B. | 图(b):n(NaOH)═3 mol时,AlCl3溶液和NaOH 溶液反应的产物 | |
| C. | 图(c):n(H2S)+n(SO2)═3 mol时,H2S与SO2反应生成的S | |
| D. | 图(d):n(HNO3)═1 mol时,Fe和稀HNO3反应生成的氧化产物(还原产物为NO) |
1.下列说法正确的是( )
①非金属氧化物一定不是碱性氧化物
②金属氧化物一定是碱性氧化物
③电解质的电离需要通电
④Fe(OH)3、FeCl2、CaSiO3 都能直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
⑥SO2可形成酸雨,酸雨的PH小于5.6.
①非金属氧化物一定不是碱性氧化物
②金属氧化物一定是碱性氧化物
③电解质的电离需要通电
④Fe(OH)3、FeCl2、CaSiO3 都能直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
⑥SO2可形成酸雨,酸雨的PH小于5.6.
| A. | ①②④ | B. | ②⑤⑥ | C. | ①④⑥ | D. | 全部 |
20.下列反应的离子方程式正确的是( )
| A. | 过氧化钠溶于水:2O22-+2H2O═4OH-+O2↑ | |
| B. | 用小苏打治疗胃酸过多:CO32-+2H+═CO2↑+H2O | |
| C. | 硫酸铜与Ba(OH)2溶液反应:Cu2++2OH-═Cu(OH)2↓ | |
| D. | 碳酸氢钠与少量Ca(OH)2溶液反应:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O |
19.关于如图装置所示的两个实验,说法正确的是( )
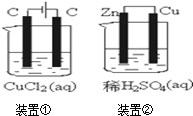

| A. | 两个装置中都发生了化学变化,都由化学能转变为电能 | |
| B. | 装置②中电流方向是从Zn经导线流入Cu | |
| C. | 反应开始阶段,两个装置中均有氢气产生 | |
| D. | 电极反应式:阳极2Cl--2e-→Cl2↑正极2H++2e-→H2↑ |
17.下列说法不正确的是( )
| A. | 利用地沟油制肥皂的实验中,可以用玻璃棒蘸取反应液滴入有热水的试管中,振荡,若无油滴浮在液面上,说明反应液中的地沟油已完全皂化 | |
| B. | 12C、13C和14C互为同位素,它们的放射性可用于考古断代,可测定生物体死亡的年代 | |
| C. | 可以利用溶液褪色的快慢来判断不同温度下同体积0.10mol•L-1酸性KMnO4溶液与0.01mol•L-1草酸稀溶液反应的快慢 | |
| D. | 燃料电池实验中,用KNO3溶液或Na2SO4溶液代替蒸馏水,效果要好得多 |
16.为了测定铁铜合金的组成,将7.6g铁、铜合金加入100mL某浓度的稀硝酸中,待合金完全溶解后,共收集到NO气体2.24L(标准状况下),并测得溶液中H+的浓度为0.5mol•L-1.若反应前后溶液的体积变化忽略不计,则下列判断正确的是( )
| A. | 上述反应中金属共失去电子0.1 mol | |
| B. | 合金中,铜的质量为2.8 g | |
| C. | 原硝酸的浓度:c(HNO3)=4.5 mol•L-1 | |
| D. | 要使溶液中的金属离子完全沉淀,需加5 mol•L-1的NaOH溶液60 mL |
15.下列有机化学方程式书写正确的是( )
0 154169 154177 154183 154187 154193 154195 154199 154205 154207 154213 154219 154223 154225 154229 154235 154237 154243 154247 154249 154253 154255 154259 154261 154263 154264 154265 154267 154268 154269 154271 154273 154277 154279 154283 154285 154289 154295 154297 154303 154307 154309 154313 154319 154325 154327 154333 154337 154339 154345 154349 154355 154363 203614
| A. | CH4+Cl$\stackrel{光照}{→}$CH2Cl2+H2 | |
| B. | H2C=CH2+Br2→CH3CHBr2 | |
| C. | 2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O | |
| D. | CH3COOCH2CH3$→_{△}^{稀硫酸}$CH3COOH+CH3CH2OH |
 ;另一种没有支链且能被氧化成醛,写出它与乙酸发生酯化反应的方程式CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH2CH2CH3+H2O.
;另一种没有支链且能被氧化成醛,写出它与乙酸发生酯化反应的方程式CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH2CH2CH3+H2O.
 .
.