4.下列过程中,一定需要通电才能实现的是( )
| A. | 电解质电离 | B. | 电化学防腐 | C. | 蓄电池放电 | D. | 电解精炼铜 |
3.根据原子结构或元素周期律的知识,下列说法正确的是( )
| A. | 35Cl和37Cl中子数不同,所以它们的原子结构示意图、电子式、核外电子排布式、轨道表达式都不相同 | |
| B. | 两个不同原子的1s、2s、2p、3s、3P各亚层中电子的能量相同 | |
| C. | 短周期主族元素原子最外层电子数一定等于其最高化合价 | |
| D. | CO2通入Na2SiO3溶液中可以得到硅酸 |
2.下列陈述I、II正确并且有因果关系的是( )
| 选项 | 陈述I | 陈述II |
| A | 油脂和汽油都是油 | 一定条件下都能发生皂化反应 |
| B | CuSO4可以用作游泳池消毒剂 | 铜盐能使蛋白质变性 |
| C | 蔗糖、淀粉、纤维素是还原性糖 | 它们一定条件下都能发生银镜反应 |
| D | 蛋白质结构中存在肽键 | 蛋白质能表现出两性 |
| A. | A | B. | B | C. | C | D. | D |
1.下列物质的检验,其结论一定正确的是( )
| A. | 向某溶液中加入BaCl2溶液,产生白色沉淀,加入HNO3后,白色沉淀不溶解,也无其他现象,说明原溶液中一定含有SO42- | |
| B. | 向某溶液中加盐酸产生无色气体,该气体能使澄清的石灰水变浑浊,说明该溶液中一定含有CO32-或SO32- | |
| C. | 取少量久置的Na2SO3样品于试管中加水溶解,再加盐酸酸化,然后加BaCl2溶液,若加盐酸有气体产生,加BaCl2有白色沉淀产生,说明Na2SO3样品已部分被氧化 | |
| D. | 将某气体通入品红溶液中,品红溶液褪色,该气体一定是SO2 |
20.分类是化学学习和研究的常用手段,下列分类依据和结论都正确的是( )
| A. | 冰醋酸、纯碱、铜绿、生石灰分别属于酸、碱、盐、氧化物 | |
| B. | HClO、H2SO4(浓)、HNO3均具有强氧化性,都是氧化性酸 | |
| C. | Al、Al2O3、Al(OH)3均既能与盐酸反应又能与氢氧化钠反应,都属于两性化合物 | |
| D. | H2SO4、NaOH、AlCl3均为强电解质,都属于离子化合物 |
19.2015年7月31日,中国获得2022年冬奥会主办权,这将促进中国冰雪运动的发展.以下关于冰的说法正确的是( )
| A. | 等质量的0℃冰与0℃的水内能相同 | B. | 冰和可燃冰都是结晶水合物 | ||
| C. | 冰和干冰、水晶的空间结构相似 | D. | 氢键影响冰晶体的体积大小 |
18.苯甲酸广泛应用于制药和化工行业,某同学尝试用甲苯的氧化反应制备苯甲酸,反应原理:
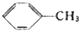 $→_{△}^{KMnO_{4}}$
$→_{△}^{KMnO_{4}}$ $\stackrel{HCl}{→}$
$\stackrel{HCl}{→}$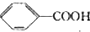
(一)制备苯甲酸
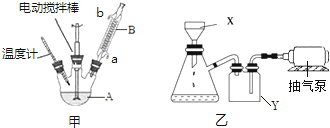
如甲图所示组装反应装置(部分装置未画出),向A中依次加入100mL水、8.5g高锰酸钾、2.7mL甲苯.相关数据如下表:
(1)装置B的作用是冷凝回流,A装置常见的规格有50mL、100mL、250mL、500mL、1000mL,最适合本实验选择的规格是250mL.
(二)分离提纯
停止加热后,按如下流程分离出苯甲酸和回收未反应的甲苯:
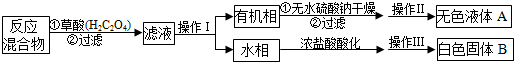
(2)操作I的名称是分液,操作Ⅱ时,应将有机相盛放在蒸馏烧瓶(填仪器名称)中.
(3)操作Ⅲ包括蒸发浓缩、冷却结晶、抽滤.抽滤装置为上图中的乙装置,将物质放在X装置(布氏漏斗)中,打开抽气泵,一段时间后X装置中剩余的是白色固体B,抽滤装置可以加快过滤速率,其工作原理是抽出装置中的空气,形成压强差,使过滤加快.
(三)提纯和纯度的测定
(4)为了进一步提纯苯甲酸,最好采用的方法是B(填编号).
A.溶于水后再过滤 B.加热升华 C.用乙醇洗涤 D.用甲苯萃取后再分液
(5)称取1.00g样品,加0.50mol/L的NaOH溶液,恰好完全反应时,消耗NaOH 溶液的体积为16.00mL,则产品的纯度为97.6%.
(四)性质验证
(6)设计实验证明苯甲酸是一种比碳酸酸性强的弱酸,简要说明实验操作,现象 和结论.
供选择的试剂:苯甲酸、苯甲酸钾溶液、饱和碳酸钠溶液、氢氧化钠溶液、稀盐酸、酚酞试液、石蕊试液.
 $→_{△}^{KMnO_{4}}$
$→_{△}^{KMnO_{4}}$ $\stackrel{HCl}{→}$
$\stackrel{HCl}{→}$
(一)制备苯甲酸

如甲图所示组装反应装置(部分装置未画出),向A中依次加入100mL水、8.5g高锰酸钾、2.7mL甲苯.相关数据如下表:
| 名称 | 相对分子质量 | 性状 | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 水 | 乙醇 | |||||
| 甲苯 | 92 | 无色液体、易燃、易挥发 | -95 | 110.6 | 不溶 | 互溶 |
| 苯甲酸 | 122 | 白色片状或针状晶体 | 112.4(100℃升华) | 248 | 微溶 | 易溶 |
(二)分离提纯
停止加热后,按如下流程分离出苯甲酸和回收未反应的甲苯:

(2)操作I的名称是分液,操作Ⅱ时,应将有机相盛放在蒸馏烧瓶(填仪器名称)中.
(3)操作Ⅲ包括蒸发浓缩、冷却结晶、抽滤.抽滤装置为上图中的乙装置,将物质放在X装置(布氏漏斗)中,打开抽气泵,一段时间后X装置中剩余的是白色固体B,抽滤装置可以加快过滤速率,其工作原理是抽出装置中的空气,形成压强差,使过滤加快.
(三)提纯和纯度的测定
(4)为了进一步提纯苯甲酸,最好采用的方法是B(填编号).
A.溶于水后再过滤 B.加热升华 C.用乙醇洗涤 D.用甲苯萃取后再分液
(5)称取1.00g样品,加0.50mol/L的NaOH溶液,恰好完全反应时,消耗NaOH 溶液的体积为16.00mL,则产品的纯度为97.6%.
(四)性质验证
(6)设计实验证明苯甲酸是一种比碳酸酸性强的弱酸,简要说明实验操作,现象 和结论.
供选择的试剂:苯甲酸、苯甲酸钾溶液、饱和碳酸钠溶液、氢氧化钠溶液、稀盐酸、酚酞试液、石蕊试液.
17.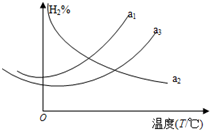 利用合成气(主要成分为CO、CO2和H2)合成甲醇,发生的主要反应如下:
利用合成气(主要成分为CO、CO2和H2)合成甲醇,发生的主要反应如下:
Ⅰ.CO(g)+2H2(g)?催化剂CH3OH(g)△H1
Ⅱ.CO2(g)+H2(g)?催化剂CO(g)+H2O(g)△H2
Ⅲ.CO2(g)+3H2(g)?催化剂CH3OH(g)+H2O(g)△H3
(1)上述反应达到平衡时对应的氢气的百分含量分别为a1、a2、a3,它们随温度变化的曲线如图所示.则△H2> (填“>”、“<”或“=”) 0,判断理由是升温平衡向吸热反应方向进行;△H1<△H3(填“>”、“<”或“=”).
(2)在温度T时,向某容器中充入1mol CO2和3mol H2,发生反应Ⅲ的反应.
①如果该容器为恒压容器,维持体系总压强p恒定,达到平衡时,已知H2的转化率为75%,则在该温度下平衡常数Kp=$\frac{100{P}^{2}}{3}$(用平衡分压代替平衡浓度计算,
分压=总压×物质的量分数).
②如果该容器为恒容容器,达到平衡时,H2的转化率<(填“>”、“<”或“=”)75%,理由是恒容容器中,达到平衡时体系压强比恒压容器中小.
(3)在2.0L密闭容器中放入1molCO2(g)和1molH2(g),在一定温度下发生反应Ⅱ的反应,2小时后达到平衡.下表为c(CO2)与反应时间的数据:
40min时,用CO2表示的该反应速率为0.008mol/L•min,分析该反应过程中c(CO2)变化与时间间隔(△t)的规律,得出的结论是随时间增加,二氧化碳浓度减少,反应速率减小.
 利用合成气(主要成分为CO、CO2和H2)合成甲醇,发生的主要反应如下:
利用合成气(主要成分为CO、CO2和H2)合成甲醇,发生的主要反应如下:Ⅰ.CO(g)+2H2(g)?催化剂CH3OH(g)△H1
Ⅱ.CO2(g)+H2(g)?催化剂CO(g)+H2O(g)△H2
Ⅲ.CO2(g)+3H2(g)?催化剂CH3OH(g)+H2O(g)△H3
(1)上述反应达到平衡时对应的氢气的百分含量分别为a1、a2、a3,它们随温度变化的曲线如图所示.则△H2> (填“>”、“<”或“=”) 0,判断理由是升温平衡向吸热反应方向进行;△H1<△H3(填“>”、“<”或“=”).
(2)在温度T时,向某容器中充入1mol CO2和3mol H2,发生反应Ⅲ的反应.
①如果该容器为恒压容器,维持体系总压强p恒定,达到平衡时,已知H2的转化率为75%,则在该温度下平衡常数Kp=$\frac{100{P}^{2}}{3}$(用平衡分压代替平衡浓度计算,
分压=总压×物质的量分数).
②如果该容器为恒容容器,达到平衡时,H2的转化率<(填“>”、“<”或“=”)75%,理由是恒容容器中,达到平衡时体系压强比恒压容器中小.
(3)在2.0L密闭容器中放入1molCO2(g)和1molH2(g),在一定温度下发生反应Ⅱ的反应,2小时后达到平衡.下表为c(CO2)与反应时间的数据:
| 反应时间t/min | 20 | 40 | 60 | 80 |
| c(CO2)(mol/L) | 0.300 | 0.180 | 0.109 | 0.066 |
16.X、Y、Z、W是元素周期表中前20号元素,且原子序数依次增大.X的一种核素在考古时常有来鉴定一些文物的年代;Y的最外层电子数是核外电子层数的3倍;Z元素的最高正价与负价代数和为6;W在前20号元素中的金属性最强.则下列说法正确的是( )
| A. | Z、W简单离子半径大小关系:W>Z | |
| B. | X、Y、Z氢化物的稳定性强弱关系:X>Y>Z | |
| C. | X可与Y和Z分别形成共价化合物 | |
| D. | Y是活泼非金属,与W形成的化合物中不可能含共价键 |
15.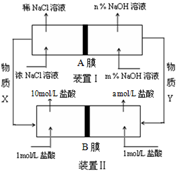 将氯碱工业与燃料电池联合能够有效降低能源消耗,如图是该工艺的图示(电源及电极未标出),则下列说法错误的是( )
将氯碱工业与燃料电池联合能够有效降低能源消耗,如图是该工艺的图示(电源及电极未标出),则下列说法错误的是( )
0 154132 154140 154146 154150 154156 154158 154162 154168 154170 154176 154182 154186 154188 154192 154198 154200 154206 154210 154212 154216 154218 154222 154224 154226 154227 154228 154230 154231 154232 154234 154236 154240 154242 154246 154248 154252 154258 154260 154266 154270 154272 154276 154282 154288 154290 154296 154300 154302 154308 154312 154318 154326 203614
 将氯碱工业与燃料电池联合能够有效降低能源消耗,如图是该工艺的图示(电源及电极未标出),则下列说法错误的是( )
将氯碱工业与燃料电池联合能够有效降低能源消耗,如图是该工艺的图示(电源及电极未标出),则下列说法错误的是( )| A. | 装置I为电解池,装置II为原电池 | |
| B. | 物质X为氯气,物质Y为氢气 | |
| C. | A膜为阳离子交换膜,B膜为阴离子交换膜 | |
| D. | 装置Ⅰ中,m小于n,装置II中a等于1 |