12.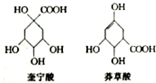 奎宁酸和莽草酸是某些高等植物特有的脂环状有机酸,常共存在一起,其结构简式如图所示.下列说法不正确的是( )
奎宁酸和莽草酸是某些高等植物特有的脂环状有机酸,常共存在一起,其结构简式如图所示.下列说法不正确的是( )
 奎宁酸和莽草酸是某些高等植物特有的脂环状有机酸,常共存在一起,其结构简式如图所示.下列说法不正确的是( )
奎宁酸和莽草酸是某些高等植物特有的脂环状有机酸,常共存在一起,其结构简式如图所示.下列说法不正确的是( )| A. | 奎宁酸的相对分子质量比莽草酸的大18 | |
| B. | 可用高锰酸钾溶液鉴别奎宁酸和莽草酸 | |
| C. | 等物质的量的奎宁酸和莽草酸分别与足量Na反应,同温同压下产生H2的体积比为4:5 | |
| D. | 等物质的量的两种分别与足量NaOH溶液反应,消耗NaOH的物质的量相同 |
11.下列实验装置不能达到目的是( )
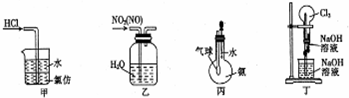

| A. | 装置甲:用于吸收HCl气体 | B. | 装置乙:用于除去NO2中的NO | ||
| C. | 装置丙:可验证氨气极易溶于水 | D. | 装置丁:可形成喷泉 |
10.化学与生产、生活、科技、环境等密切相关,下列说法不正确的是( )
| A. | 用蘸有浓氨水的棉棒检验输送氯气的管道是否漏气 | |
| B. | 用合成聚碳酸酯可降解塑料,实现“碳”的循环利用 | |
| C. | 大力实施矿物燃料脱硫脱硝技术,能减少二氧化硫、氮氧化物的排放 | |
| D. | 向工业生产的反应中加入合适的催化剂,能改变反应的焓变 |
9.浓硫酸与下列物质作用时,既表现氧化性,又表现酸性的是( )
①炽热的木炭 ②H2S气体 ③Cu ④FeO ⑤NH3 ⑥蔗糖 ⑦CuSO4•5H2O ⑧铁、铝.
①炽热的木炭 ②H2S气体 ③Cu ④FeO ⑤NH3 ⑥蔗糖 ⑦CuSO4•5H2O ⑧铁、铝.
| A. | ③④ | B. | ①②⑤⑧ | C. | ①②③④⑦ | D. | ⑥⑦ |
6.在常温下,下列溶液不能溶解铁的是( )
| A. | 稀硫酸 | B. | FeCl3溶液 | C. | CuCl2 | D. | 浓硝酸 |
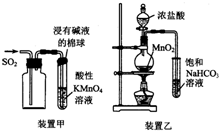
3.下列有关实验原理或实验操作正确的是( )
0 154103 154111 154117 154121 154127 154129 154133 154139 154141 154147 154153 154157 154159 154163 154169 154171 154177 154181 154183 154187 154189 154193 154195 154197 154198 154199 154201 154202 154203 154205 154207 154211 154213 154217 154219 154223 154229 154231 154237 154241 154243 154247 154253 154259 154261 154267 154271 154273 154279 154283 154289 154297 203614

| A. | 用装置甲收集SO2并验证其漂白性 | |
| B. | 用装置乙验证氯气与水反应有盐酸生成 | |
| C. | 用澄清石灰水鉴别苏打溶液和小苏打溶液 | |
| D. | 用NaOH溶液除去苯中混有的少量苯酚,反应后分液 |

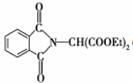 .
.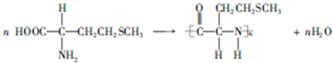 .
.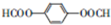 .
.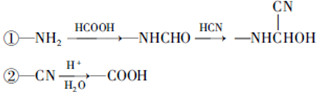
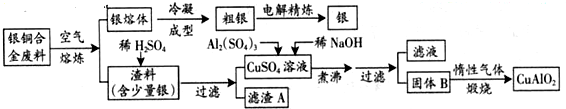
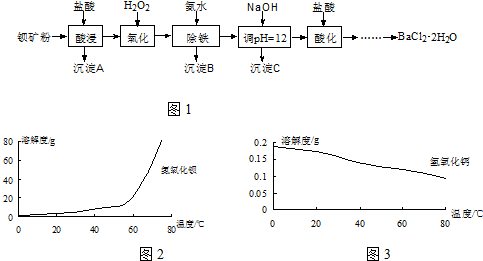
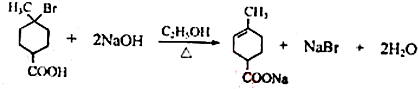
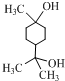
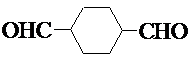
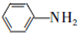 和HCOOH为原料制备化合物
和HCOOH为原料制备化合物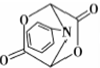 的流程如下:
的流程如下: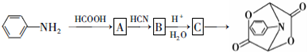
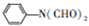 ,C
,C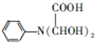 .
.
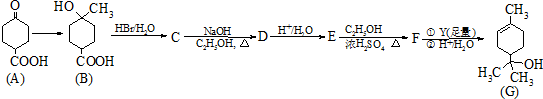
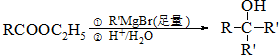
 .
.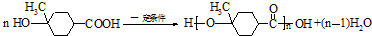 .
. .
. .
.