题目内容
3.下列有关实验原理或实验操作正确的是( )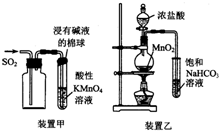
| A. | 用装置甲收集SO2并验证其漂白性 | |
| B. | 用装置乙验证氯气与水反应有盐酸生成 | |
| C. | 用澄清石灰水鉴别苏打溶液和小苏打溶液 | |
| D. | 用NaOH溶液除去苯中混有的少量苯酚,反应后分液 |
分析 A.二氧化硫有还原性;
B.氯化氢易挥发;
C.氢氧化钙和碳酸根离子、碳酸氢根离子都生成碳酸钙沉淀;
D.氢氧化钠与苯酚反应生成苯酚钠,苯酚钠溶于水,苯不与水互溶.
解答 解:A.二氧化硫有还原性,能使酸性高锰酸钾褪色,故A错误;
B.氯化氢易挥发,应除掉后再检验,故B错误;
C.Na2CO3+Ca(OH)2═CaCO3↓+2NaOH、2NaHCO3+Ca(OH)2═CaCO3↓+Na2CO3+2H2O,都出现白色沉淀,无法鉴别,故C错误;
D.氢氧化钠与苯酚反应生成苯酚钠,苯酚钠溶于水,苯不与水互溶,通过反应进行分离,故D正确.
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及物质的检验、分离提纯及物质的性质等,难度不大,注意基础知识的理解掌握.

练习册系列答案
 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
11.短周期元素A、B、C、D在周期表中的位置如图所示,B、D最外层电子数之和为12.回答下列问题:
(1)与元素B、D处于同一主族的第2-5周期元素单质分别与H2反应生成1mol气态氢化物对应的热量变化如下,其中能表示该主族第4周期元素的单质生成1mol气态氢化物所对应的热量变化是b(选填字母编号).
a.吸收99.7kJ b.吸收29.7kJ c.放出20.6kJ d.放出241.8kJ
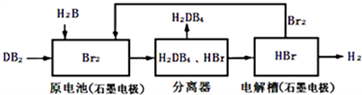
(2)DB2通过下列工艺流程可制化工业原料H2DB4和清洁能源H2.
①查得:
试写出通常条件下电解槽中发生总反应的热化学方程式:2HBr(aq)=H2(g)+Br2(g)△H=+94kJ/mol
②根据资料:
为检验分离器的分离效果,取分离后的H2DB4溶液于试管,向其中逐滴加入AgNO3溶液至充分反应,若观察到无淡黄色沉淀产生,最终生成白色沉淀,证明分离效果较好.
③在原电池中,负极发生的反应式为SO2+2H2O-2e-=4H++SO42-.
④在电解过程中,电解槽阴极附近溶液pH变大(填“变大”、“变小”或“不变”).
⑤将该工艺流程用总反应的化学方程式表示为:SO2+2H2O=H2+H2SO4.该生产工艺的优点有Br2被循环利用或能源循环供给或获得清洁能源(答一点即可).
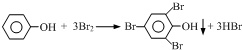
(3)溴及其化合物广泛应用于医药、农药、纤维、塑料阻燃剂等,回答下列问题:海水提溴过程中,向浓缩的海水中通入Cl2,将其中的Br-氧化,再用空气吹出溴;然后用碳酸钠溶液吸收溴,溴歧化为Br-和BrO3-,其离子方程式为3 Br2+6 CO32-+3H2O=5 Br-+BrO3-+6HCO3-(或3 Br2+3CO32-=5 Br-+BrO3-+3CO2↑).
| A | B | |
| C | D |
a.吸收99.7kJ b.吸收29.7kJ c.放出20.6kJ d.放出241.8kJ
(2)DB2通过下列工艺流程可制化工业原料H2DB4和清洁能源H2.

①查得:
| 化学键 | H-H | Br-Br | H-Br |
| 键能(kJ/mol) | 436 | 194 | 362 |
②根据资料:
| 化学式 | Ag2SO4 | AgBr |
| 溶解度(g) | 0.796 | 8.4×10-6 |
③在原电池中,负极发生的反应式为SO2+2H2O-2e-=4H++SO42-.
④在电解过程中,电解槽阴极附近溶液pH变大(填“变大”、“变小”或“不变”).
⑤将该工艺流程用总反应的化学方程式表示为:SO2+2H2O=H2+H2SO4.该生产工艺的优点有Br2被循环利用或能源循环供给或获得清洁能源(答一点即可).
(3)溴及其化合物广泛应用于医药、农药、纤维、塑料阻燃剂等,回答下列问题:海水提溴过程中,向浓缩的海水中通入Cl2,将其中的Br-氧化,再用空气吹出溴;然后用碳酸钠溶液吸收溴,溴歧化为Br-和BrO3-,其离子方程式为3 Br2+6 CO32-+3H2O=5 Br-+BrO3-+6HCO3-(或3 Br2+3CO32-=5 Br-+BrO3-+3CO2↑).
18.下列离子方程式错误的是( )
| A. | 二氧化硅与苛性钠反应:SiO2+2OH-═SiO32-+H2O | |
| B. | 在NaCl溶液中滴入AgNO3试液:Ag++Cl-═AgCl↓ | |
| C. | Cl2溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 用NaOH溶液吸收Cl2:Cl2+2OH-═Cl-+ClO-+H2O |
15. 乙酰苯胺是常用的医药中间体,可由苯胺与乙酸制备.反应的化学方程式如下:
乙酰苯胺是常用的医药中间体,可由苯胺与乙酸制备.反应的化学方程式如下:
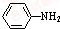 (苯胺)+CH3COOH?
(苯胺)+CH3COOH? (乙酸苯胺)+H2O
(乙酸苯胺)+H2O
有关化合物的物理性质见下表:
合成:
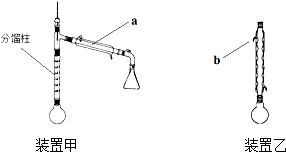
方案甲:采用装置甲(分馏柱的作用类似于石油分馏中的分馏塔).在圆底烧瓶中加入5.0mL 苯胺、7.4mL乙酸,加热至沸,控制温度计读数100~105℃,保持液体平缓流出,反应40min后停止加热.将圆底烧瓶中的液体趁热倒入盛有100mL水的烧杯,冷却后有乙酰苯胺固体析出,过滤得粗产物.
方案乙:采用装置乙,加热回流,反应40min后停止加热.其余与方案甲相同.
提纯:
甲乙两方案均采用重结晶方法.操作如下:
①加热溶解→②活性炭脱色→③趁热过滤→④冷却结晶→⑤过滤→⑥洗涤→⑦干燥
请回答:
(1)仪器a的名称是冷凝管,b处水流方向是出水(填“进水”或“出水”).
(2)合成步骤中,乙酰苯胺固体析出后,过滤分离出粗产物.留在滤液中的主要物质是乙酸.
(3)提纯过程中的第③步,过滤要趁热的理由是防止温度降低导致乙酰苯胺析出,降低产率.
(4)提纯过程第⑥步洗涤,下列洗涤剂中最合适的是A.
A.蒸馏水 B.乙醇 C.5%Na2CO3溶液 D.饱和NaCl溶液
(5)从投料量分析,为提高乙酰苯胺产率,甲乙两种方案均采取的措施是乙酸过量;实验结果表明方案甲的产率较高,原因是方案甲将反应过程中生成的水蒸出,促进反应.
 乙酰苯胺是常用的医药中间体,可由苯胺与乙酸制备.反应的化学方程式如下:
乙酰苯胺是常用的医药中间体,可由苯胺与乙酸制备.反应的化学方程式如下: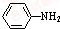 (苯胺)+CH3COOH?
(苯胺)+CH3COOH? (乙酸苯胺)+H2O
(乙酸苯胺)+H2O有关化合物的物理性质见下表:
| 化合物 | 密度(g.cm-3) | 溶解性 | 熔点(℃) | 沸点(℃) |
| 乙酸 | 1.05 | 易溶于水、乙醇 | 17 | 118 |
| 苯胺 | 1.02 | 微溶于水,易溶于乙醇 | -6 | 184 |
| 乙酰苯胺 | - | 微溶于冷水,可溶于热水,易溶于乙醇 | 114 | 304 |
方案甲:采用装置甲(分馏柱的作用类似于石油分馏中的分馏塔).在圆底烧瓶中加入5.0mL 苯胺、7.4mL乙酸,加热至沸,控制温度计读数100~105℃,保持液体平缓流出,反应40min后停止加热.将圆底烧瓶中的液体趁热倒入盛有100mL水的烧杯,冷却后有乙酰苯胺固体析出,过滤得粗产物.
方案乙:采用装置乙,加热回流,反应40min后停止加热.其余与方案甲相同.
提纯:
甲乙两方案均采用重结晶方法.操作如下:
①加热溶解→②活性炭脱色→③趁热过滤→④冷却结晶→⑤过滤→⑥洗涤→⑦干燥
请回答:
(1)仪器a的名称是冷凝管,b处水流方向是出水(填“进水”或“出水”).
(2)合成步骤中,乙酰苯胺固体析出后,过滤分离出粗产物.留在滤液中的主要物质是乙酸.
(3)提纯过程中的第③步,过滤要趁热的理由是防止温度降低导致乙酰苯胺析出,降低产率.
(4)提纯过程第⑥步洗涤,下列洗涤剂中最合适的是A.
A.蒸馏水 B.乙醇 C.5%Na2CO3溶液 D.饱和NaCl溶液
(5)从投料量分析,为提高乙酰苯胺产率,甲乙两种方案均采取的措施是乙酸过量;实验结果表明方案甲的产率较高,原因是方案甲将反应过程中生成的水蒸出,促进反应.
13.下列反应的离子方程式书写正确的是( )
| A. | 石灰石与盐酸反应:CO32-+2H+=H2O+CO2↑ | |
| B. | 氯化铝溶液与氨水反应:Al3++3OH-=Al(OH)3↓ | |
| C. | 铁粉与硝酸银溶液反应:Fe+3Ag+=Fe3++3Ag | |
| D. | 醋酸与氢氧化钠溶液反应:CH3COOH+OH-=CH3COO-+H2O |